Aktivní složky: kyselina alendronová, cholekalciferol
ADROVANCE 70 mg / 2 800 IU tablety
ADROVANCE 70 mg / 5 600 IU tablety
Proč se používá Adrovance? K čemu to je?
Co je ADROVANCE?
ADROVANCE je tableta, která obsahuje dvě léčivé látky, kyselinu alendronovou (běžně nazývanou alendronát) a cholekalciferol, známý jako vitamín D3.
Co je alendronát?
Alendronát patří do skupiny nehormonálních léčiv nazývaných bisfosfonáty. Alendronát zabraňuje ztrátě kostní hmoty, ke které dochází u postmenopauzálních žen, a pomáhá obnovovat kost. Alendronát snižuje riziko zlomenin obratlů a páteře. “Kyčle.
Co je vitamín D?
Vitamín D je základní živinou potřebnou pro vstřebávání vápníku a zdraví kostí. Tělo dokáže vápník z potravy dostatečně absorbovat, pouze pokud má dostatek vitaminu D. Potravin obsahujících vitamín D je velmi málo. K hlavní dodávce vitaminu D dochází v létě působením slunečního světla, které v kůži produkuje vitamín D. Jak stárneme, pokožka produkuje méně vitaminu D. Příliš nízké množství vitaminu D může způsobit úbytek kostní hmoty a osteoporózu. Silný nedostatek vitaminu D může způsobit svalovou slabost, která může vést k pádům a zvýšenému riziku zlomenin ...
K čemu se ADROVANCE používá?
Váš lékař předepsal přípravek ADROVANCE k léčbě osteoporózy a ke snížení rizika nedostatečnosti vitaminu D. Tento lék snižuje riziko zlomenin páteře a kyčle u žen po menopauze.
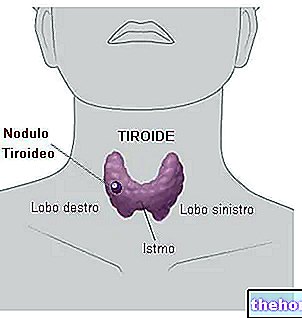
Co je osteoporóza?
Osteoporóza je řídnutí a oslabení kostí. Je to běžné u žen po menopauze. V menopauze vaječníky přestávají produkovat ženský hormon estrogen, který pomáhá udržovat zdravou kostru ženy. V důsledku toho dochází k úbytku kostní hmoty a kostní tkáni. se stává slabším. Riziko osteoporózy je tím větší, čím dříve žena dosáhne menopauzy.
V počátečních stádiích osteoporóza obvykle nemá žádné příznaky. Pokud však léčba není zahájena, mohou dojít ke zlomeninám. Ačkoli zlomeniny jsou obvykle bolestivé, zlomeniny kostí páteře nemusí být cítit, dokud nejsou nalezeny. S poklesem postavy . Ke zlomeninám může dojít při každodenních činnostech, jako je zvedání závaží, nebo při drobných poraněních, která by obvykle nemohla způsobit zlomeniny normální kosti. Zlomeniny se běžně vyskytují v kyčli, páteři nebo zápěstí a mohou být nejen bolestivé, ale mohou vést k výrazným deformitám a postižení, jako je úklony zad (hrb) a omezení pohybu.
Jak lze léčit osteoporózu?
Spolu s léčbou přípravkem ADROVANCE může lékař navrhnout změny životního stylu ke zlepšení stavu onemocnění, jako například:
- Ukončení kouření Zdá se, že kouření zvyšuje rychlost ztráty kostní hmoty, a proto může zvyšovat riziko zlomenin.
- Cvičení Stejně jako svaly, i kosti potřebují cvičení, aby zůstaly silné a zdravé. Před zahájením cvičebního programu se poraďte se svým lékařem.
- Vyvážená strava Lékař bude schopen poskytnout informace o dietě nebo o možné potřebě užívat doplňky stravy.
Kontraindikace Kdy by Adrovance neměl být používán
Neužívejte ADROVANCE
- jestliže jste alergický (á) na kyselinu alendronovou, cholekalciferol nebo na kteroukoli další složku tohoto přípravku
- pokud máte určité problémy s jícnem (trubice spojující ústa se žaludkem), jako je zúžení nebo potíže s polykáním,
- pokud nemůžete stát nebo sedět vzpřímeně alespoň 30 minut,
- pokud vám lékař řekl, že máte nízkou hladinu vápníku v krvi.
Pokud si myslíte, že se vás cokoli z výše uvedeného týká, tablety neužívejte. Poraďte se se svým lékařem a řiďte se uvedenými pokyny.
Opatření pro použití Co potřebujete vědět, než začnete Adrovance užívat
Před užitím přípravku ADROVANCE se poraďte se svým lékařem nebo lékárníkem, pokud:
- trpíte problémy s ledvinami,
- máte nebo jste nedávno měl / a potíže s polykáním nebo problémy s trávicím systémem,
- Váš lékař vám řekl, že máte Barrettův jícen (onemocnění spojené se změnami buněk, které lemují spodní část jícnu),
- Váš lékař vám řekl, že máte problém se vstřebáváním minerálů v žaludku nebo střevech (malabsorpční syndrom),
- máte špatné zubní zdraví, trpíte onemocněním dásní, plánujete extrakci zubu nebo nepodstupujete pravidelné zubní prohlídky,
- má rakovinu,
- podstupujete chemoterapii nebo radioterapii,
- užíváte inhibitory angiogeneze (jako je bevacizumab nebo thalidomid), které se používají k léčbě rakoviny,
- užíváte kortikosteroidy (jako je prednison nebo dexamethason), které se používají k léčbě stavů, jako je astma, revmatoidní artritida a závažné alergie,
- jste nebo jste byli kuřáci (protože to může zvýšit riziko problémů se zuby).
Před zahájením léčby přípravkem ADROVANCE můžete být požádáni o zubní prohlídku.
Během léčby přípravkem ADROVANCE je důležité udržovat dobrou ústní hygienu. Po celou dobu léčby byste měli absolvovat pravidelné prohlídky u zubaře a měli byste kontaktovat svého lékaře nebo zubaře, pokud se u vás objeví jakýkoli typ problému v ústech nebo zubech, jako je uvolnění, bolest nebo otok.
Může dojít k podráždění, zánětu nebo ulceraci jícnu (trubice spojující ústa se žaludkem) často s příznaky bolesti na hrudi, pálení žáhy, obtíží nebo bolesti při polykání, zvláště pokud pacienti nepijí plnou sklenici vody z vodovodu a / nebo se protáhnout během prvních 30 minut po užití přípravku ADROVANCE Tyto nežádoucí účinky se mohou zhoršit, pokud pacienti pokračují v užívání přípravku ADROVANCE i po výskytu těchto příznaků.
Děti a dospívající
ADROVANCE by neměl být podáván dětem a mladistvým do 18 let.
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Adrovance
Další léčivé přípravky a ADROVANCE
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval (a) nebo které možná budete užívat.
Doplňky vápníku, antacida a některé perorálně podávané léky pravděpodobně interferují s absorpcí přípravku ADROVANCE, pokud jsou užívány současně. Je proto důležité počkat alespoň 30 minut, než začnete užívat jakékoli jiné perorálně podávané léky nebo doplňky.
Některé dlouhodobé léky proti bolesti nebo revmatismu nazývané NSAID (např. Kyselina acetylsalicylová nebo ibuprofen) mohou způsobit zažívací potíže. Proto je při podávání těchto léčivých přípravků souběžně s přípravkem ADROVANCE zapotřebí opatrnosti.
Je pravděpodobné, že některé léky nebo potravinářské přídatné látky mohou zabránit vniknutí vitaminu D obsaženého v přípravku ADROVANCE do vašeho těla, včetně umělých náhražek tuků, minerálních olejů, léků na hubnutí, orlistatu a léků snižujících hladinu cholesterolu, cholestyraminu a cholestipolu na záchvaty (epilepsie) (jako je fenytoin nebo fenobarbital) mohou snižovat účinnost vitaminu D. Lze zvážit přidání dalších doplňků vitaminu D na individuální bázi.
ADROVANCE s jídlem a pitím
Jídlo a nápoje (včetně minerální vody) pravděpodobně sníží účinnost přípravku ADROVANCE, pokud jsou užívány současně. Musíte počkat alespoň 30 minut, než si vezmete jídlo a pití jiné než vodu z vodovodu.
Varování Je důležité vědět, že:
Těhotenství a kojení
ADROVANCE je indikován pouze u postmenopauzálních žen. Neužívejte ADROVANCE, pokud jste těhotná nebo těhotná nebo pokud kojíte.
Řízení dopravních prostředků nebo obsluha strojů
U přípravku ADROVANCE byly hlášeny nežádoucí účinky (např. Rozmazané vidění, závratě a silná bolest kostí, svalů nebo kloubů), které mohou ovlivnit schopnost řídit nebo obsluhovat stroje.Pokud se kterýkoli z těchto nežádoucích účinků vyskytne, neměli byste řídit, dokud se necítíte dobře.
ADROVANCE obsahuje laktózu a sacharózu
Pokud vám lékař řekl, že nesnášíte některé cukry, kontaktujte svého lékaře před užitím tohoto léčivého přípravku.
Dávka, způsob a doba podání Jak používat Adrovance: Dávkování
Vždy užívejte přípravek ADROVANCE přesně podle pokynů svého lékaře nebo lékárníka. Pokud máte pochybnosti, poraďte se se svým lékařem nebo lékárníkem.
Užívejte jednu tabletu ADROVANCE jednou týdně.
Postupujte pečlivě podle níže uvedených pokynů:
- Vyberte si den v týdnu, který nejlépe odpovídá vašim aktivitám. Užívejte jednu tabletu ADROVANCE jednou týdně ve zvolený den. Je velmi důležité, abyste dodržovali pokyny 2), 3), 4) a 5), abyste usnadnili rychlý vstup tablety ADROVANCE do žaludku a pomohli snížit možnost podráždění jícnu (trubice, která spojuje vaše ústa s žaludek).
- Poté, co vstanete z postele, začnete den a než si vezmete jídlo, pití nebo jiný lék, spolkněte tabletu ADROVANCE celou a zapijte plnou sklenicí vody z vodovodu (ne minerální vody) (ne méně než 200 ml), aby byl přípravek ADROVANCE dostatečně absorbováno. Neužívejte s minerální vodou (neperlivou ani perlivou). Neužívejte s kávou nebo čajem. Neužívejte se šťávou nebo mlékem.
- Tabletu nedrťte ani nežvýkejte ani nenechávejte rozpustit v ústech kvůli možné tvorbě vředů v ústní dutině.
- Nelehejte - držte trup ve vzpřímené poloze (vsedě, ve stoje nebo při chůzi) - alespoň 30 minut po požití tablety. Neuvolňujte se, dokud něco nesníte.
- ADROVANCE by neměl být užíván před spaním nebo před vstáváním z postele na začátku dne. svého lékaře.
- Po spolknutí tablety ADROVANCE počkejte alespoň 30 minut, než budete jíst, pít nebo užívat jiné léky dne, včetně antacid, doplňků vápníku a vitamínů. ADROVANCE je účinný pouze tehdy, když se užívá na prázdný žaludek.
Jestliže jste zapomněl (a) užít ADROVANCE
Pokud zapomenete užít tabletu, jednoduše užijte jednu tabletu ADROVANCE druhý den ráno. Neužívejte dvě tablety ve stejný den. Poté pokračujte v užívání tablety ve zvolený den v týdnu.
Jestliže jste přestal (a) užívat přípravek ADROVANCE
Je důležité, abyste přípravek ADROVANCE užívali tak dlouho, jak vám předepisuje lékař. Vzhledem k tomu, že není známo, jak dlouho byste měli přípravek ADROVANCE užívat, měli byste se u svého lékaře pravidelně informovat o nutnosti pokračovat v užívání tohoto léku, abyste zjistili, zda je přípravek ADROVANCE pro vás stále vhodný.
Návod na použití je součástí balení přípravku ADROVANCE a obsahuje důležité informace, které vám připomínají, jak správně užívat přípravek ADROVANCE.
Máte -li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
Předávkování Co dělat, když jste užil příliš mnoho přípravku Adrovance
Pokud omylem užijete příliš mnoho tablet, vypijte plnou sklenici mléka a okamžitě kontaktujte svého lékaře. Nevyvolávejte zvracení a nelehejte.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Adrovance
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Okamžitě navštivte svého lékaře, pokud si všimnete některého z následujících nežádoucích účinků, které mohou být závažné a u kterých můžete potřebovat naléhavou lékařskou péči:
Časté (mohou postihnout až 1 z 10 lidí):
- pálení žáhy v horní části žaludku; potíže s polykáním; bolest při polykání; vředy v jícnu (trubice spojující ústa se žaludkem), které mohou způsobit bolest na hrudi, pálení žáhy nebo potíže nebo bolest při polykání.
Vzácné (mohou postihnout až 1 z 1000 lidí):
- alergické reakce, jako je kopřivka; otok obličeje, rtů, jazyka a / nebo hrdla, pravděpodobně způsobující potíže s dýcháním nebo polykáním; závažné kožní reakce,
- bolest v ústech a / nebo čelisti, otok nebo vředy v ústech, necitlivost nebo pocit těžkosti v čelisti nebo uvolnění zubu. Mohou to být známky poškození kosti v čelisti (osteonekróza) obvykle spojené s opožděným hojením a infekce, často po extrakci zubu. Pokud se u vás tyto příznaky objeví, kontaktujte svého lékaře a zubaře.
- neobvykle může dojít k neobvyklé zlomenině stehenní kosti, zvláště u pacientů dlouhodobě léčených na osteoporózu. Kontaktujte svého lékaře, pokud pociťujete bolest, slabost nebo nepohodlí ve stehně, kyčli nebo tříslech, protože to může být časná indikace. možné zlomeniny stehenní kosti,
- bolest kostí, svalů a / nebo kloubů, která je závažná.
Mezi další nežádoucí účinky patří
Velmi časté (mohou postihnout více než 1 z 10 lidí):
- bolest kostí, svalů a / nebo kloubů, která je někdy závažná.
Časté (mohou postihnout až 1 z 10 lidí):
- otok kloubů,
- bolest břicha; žaludeční nevolnost nebo říhání po jídle; zácpa; pocit plnosti nebo nadýmání v žaludku; průjem, střevní plyn,
- ztráta vlasů; svědění,
- bolest hlavy; závrať,
- únava; otok rukou nebo nohou.
Méně časté (mohou postihnout až 1 ze 100 lidí):
- nevolnost; Vyděsil,
- podráždění nebo zánět jícnu (trubice, která spojuje vaše ústa se žaludkem) nebo žaludku,
- černá nebo tmavá stolice,
- rozmazané vidění; bolest očí nebo zarudnutí,
- vyrážka; zarudnutí kůže,
- přechodné příznaky podobné chřipce, jako jsou bolesti těla, celkový pocit nevolnosti a někdy s horečkou, obvykle na začátku léčby,
- změna chuti.
Vzácné (mohou postihnout až 1 z 1000 lidí):
- příznaky nízké hladiny vápníku v krvi včetně svalových křečí nebo křečí a / nebo mravenčení v prstech nebo kolem úst,
- žaludeční nebo peptické vředy (někdy závažné nebo s krvácením),
- zúžení jícnu (trubice, která spojuje vaše ústa se žaludkem),
- vyrážka zhoršená vystavením slunečnímu záření,
- vředy v ústech.
Velmi vzácné (mohou postihnout až 1 z 10 000 lidí):
- poraďte se se svým lékařem, pokud máte bolesti ucha, výtok z ucha a / nebo ušní infekci.Tyto epizody mohou být známkami poškození kosti v uchu.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi.
Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48100 41 Praha 10 Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
Expirace a retence
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce a blistru za EXP. Datum exspirace se vztahuje k poslednímu dni uvedeného měsíce.
Uchovávejte v původním blistru, aby byl přípravek chráněn před vlhkostí a světlem.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Jiná informace
Jaká ADROVANCE
Léčivými látkami jsou kyselina alendronová a cholekalciferol (vitamin D3). Jedna tableta ADROVANCE 70 mg / 2800 IU obsahuje 70 mg kyseliny alendronové (ve formě trihydrátu sodíku) a 70 mikrogramů (2800 IU) cholekalciferolu (vitamin D3). Jedna tableta ADROVANCE 70 mg / 5 600 IU obsahuje 70 mg kyseliny alendronové (ve formě trihydrátu sodíku) a 140 mikrogramů (5 600 IU) cholekalciferolu (vitamin D3).
Dalšími složkami jsou mikrokrystalická celulóza (E460), bezvodá laktóza (viz bod 2), triglyceridy se středním řetězcem, želatina, sodná sůl kroskarmelózy, sacharóza (viz bod 2), koloidní oxid křemičitý, stearát hořečnatý (E572), butylhydroxytoluen (E321), modifikovaný škrob (kukuřice) a křemičitan hlinito -sodný (E554).
Jak ADROVANCE vypadá a obsah balení
Tablety ADROVANCE 70 mg / 2 800 IU jsou k dispozici jako bílé až téměř bílé, upravené tablety ve tvaru tobolky, s vyraženým obrysem kostního obrazu na jedné straně a „710“ na druhé straně. Tablety ADROVANCE 70 mg / 2 800 IU jsou k dispozici v baleních obsahujících 2, 4, 6 nebo 12 tablet.
Tablety ADROVANCE 70 mg / 5 600 IU jsou k dispozici jako upravené, obdélníkové, bílé až téměř bílé tablety s vyraženým obrysem kostního obrazu na jedné straně a „270“ na druhé straně. Tablety ADROVANCE 70 mg / 5 600 IU jsou k dispozici v baleních obsahujících 2, 4 nebo 12 tablet.
Na trhu nemusí být všechny velikosti balení.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky).Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
ADROVANCE
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
ADROVANCE 70 mg / 2 800 IU tablety
Jedna tableta obsahuje 70 mg kyseliny alendronové (jako trihydrát sodný) a 70 mcg (2 800 IU) cholekalciferolu (vitamín D3).
Pomocné látky se známými účinky
Jedna tableta obsahuje 62 mg laktózy (jako bezvodé laktózy) a 8 mg sacharózy.
ADROVANCE 70 mg / 5 600 IU tablety
Jedna tableta obsahuje 70 mg kyseliny alendronové (jako trihydrát sodný) a 140 mcg (5600 IU) cholekalciferolu (vitamín D3).
Pomocné látky se známými účinky
Jedna tableta obsahuje 63 mg laktózy (jako bezvodé laktózy) a 16 mg sacharózy.
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Tableta.
ADROVANCE 70 mg / 2 800 IU tablety
Upravené bílé až téměř bílé tablety ve tvaru tobolky s vyraženým obrysem kostního obrazu na jedné straně a „710“ na druhé straně.
ADROVANCE 70 mg / 5 600 IU tablety
Bílé až téměř bílé, tablety obdélníkového tvaru s vyraženým obrysem obrázku kosti na jedné straně a „270“ na druhé straně.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
ADROVANCE je indikován k léčbě postmenopauzální osteoporózy u žen s rizikem nedostatku vitaminu D. Snižuje riziko zlomenin obratlů a kyčle.
04.2 Dávkování a způsob podání
Dávkování
Doporučená dávka je jedna tableta jednou týdně.
Pacienti by měli být poučeni, že pokud zapomněli užít dávku přípravku ADROVANCE, mají užít jednu tabletu ráno následujícího dne. Neměly by užít dvě tablety ve stejný den, ale měly by znovu začít užívat jednu tabletu jednou týdně, ve zvolený den, jak bylo dříve nastaveno.
Vzhledem k povaze chorobného procesu osteoporózy by měl být ADROVANCE používán jako dlouhodobá terapie.
Optimální délka léčby osteoporózy bisfosfonáty nebyla stanovena. Potřeba pokračování léčby by měla být u každého jednotlivého pacienta pravidelně přehodnocována na základě potenciálních přínosů a rizik přípravku ADROVANCE, zejména po 5 a více letech používání.
Pokud je příjem vápníku v potravě nedostatečný, měli by pacienti užívat doplňky vápníku (viz bod 4.4). Na individuálním základě by mělo být zváženo další doplnění vitaminu D s přihlédnutím k veškerému dennímu příjmu vitamínů. D užíváno s vitamíny a doplňky stravy.
ADROVANCE 70 mg / 2 800 IU tablety
Ekvivalence příjmu ADROVANCE 2800 IU vitaminu D3 jednou týdně a 400 IU vitaminu D jednou denně nebyla studována.
ADROVANCE 70 mg / 5 600 IU tablety
Ekvivalence příjmu ADROVANCE 5 600 IU vitaminu D3 jednou týdně a 800 IU vitaminu D jednou denně nebyla studována.
Senioři
V klinických studiích nebyl prokázán žádný věkově rozdílný rozdíl v profilech účinnosti nebo bezpečnosti alendronátu. U starších osob proto není nutná úprava dávky.
Porucha funkce ledvin
ADROVANCE se nedoporučuje u pacientů s poruchou funkce ledvin, pokud je clearance kreatininu nižší než 35 ml / min, protože v tomto ohledu nejsou žádné zkušenosti. U pacientů s clearance kreatininu vyšší než 35 ml / min není nutná úprava dávky.
Pediatrická populace
Bezpečnost a účinnost přípravku ADROVANCE nebyla u dětí mladších 18 let stanovena. Tento přípravek by neměl být používán u dětí mladších 18 let, protože nejsou k dispozici žádné údaje o kombinaci kyseliny alendronové / cholekalciferolu. Aktuálně dostupné údaje o kyselině alendronové u pediatrické populace jsou popsány v bodě 5.1.
Způsob podání
Perorální podání.
K získání adekvátní absorpce alendronátu:
ADROVANCE by měl být užíván pouze s vodou z vodovodu (nikoli minerální vodou) nejméně 30 minut před jakýmkoli jídlem, pitím nebo léky (včetně antacid, doplňků vápníku a vitamínů) dne. Jiné nápoje (včetně minerálních vod), potraviny a některé léčivé přípravky pravděpodobně sníží absorpci alendronátu (viz body 4.5 a 4.8).
Následující pokyny je třeba přesně dodržovat, aby se minimalizovalo riziko podráždění jícnu a souvisejících nežádoucích účinků (viz bod 4.4):
• ADROVANCE by měl být spolknut pouze poté, co vstanete z postele, abyste mohli začít den plnou sklenicí vody (ne méně než 200 ml).
• Pacient by měl polykat ADROVANCE pouze celý. Pacient by neměl tabletu drtit, žvýkat nebo rozpouštět v ústech kvůli možnému riziku orofaryngeální ulcerace.
• Pacient by si neměl lehnout alespoň 30 minut po užití přípravku ADROVANCE a pokud nic nejedl.
• ADROVANCE by neměl být užíván před spaním nebo před vstáváním z postele na začátku dne.
04.3 Kontraindikace
- Přecitlivělost na léčivé látky nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
- Poruchy jícnu a další faktory, které zpomalují vyprazdňování jícnu, jako je striktura nebo achalázie.
- Neschopnost stát nebo sedět vzpřímeně alespoň 30 minut.
- Hypokalcemie.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Alendronát
Nežádoucí reakce horního gastrointestinálního traktu
Alendronát může způsobit lokální podráždění sliznice horní části gastrointestinálního traktu. Vzhledem k možnosti zhoršení základního onemocnění je při podávání alendronátu pacientům s aktivními poruchami horní části trávicího traktu, jako je dysfagie, jícnu, gastritida, duodenitida, vředy nebo s nedávná (v předchozím roce) anamnéza závažných gastrointestinálních poruch, jako je peptický vřed nebo aktivní gastrointestinální krvácení nebo operace horního gastrointestinálního traktu s výjimkou pyloroplastiky (viz bod 4.3) .U pacientů s již známým Barrettovým jícnem by měl lékař vyhodnotit potenciální přínosy a rizika alendronát na individuálním základě.
U pacientů léčených alendronátem byly hlášeny reakce jícnu (některé závažné a vyžadující hospitalizaci), jako je ezofagitida, vředy jícnu a eroze jícnu, zřídka následované zúžením jícnu. a vyhledejte lékařskou pomoc, pokud se objeví příznaky podráždění jícnu, jako je dysfagie, odynofagie nebo retrosternální bolest nebo rozvoj nebo zhoršení pálení žáhy (viz bod 4.8).
Zdá se, že riziko závažných jícnových nežádoucích účinků je vyšší u pacientů, kteří neužívají alendronát správně a / nebo kteří pokračují v užívání alendronátu poté, co se u nich vyvinou příznaky naznačující podráždění jícnu. Je velmi důležité, aby pacient věděl a rozuměl tomu, jak lék užívat (viz bod 4.2). Pacienta je třeba upozornit, že pokud nebudou tato opatření dodržována, může se zvýšit riziko problémů s jícnem.
Přestože ve velkých klinických studiích s alendronátem nebylo pozorováno zvýšené riziko, byly hlášeny vzácné (po uvedení na trh) případy žaludečních a duodenálních vředů, některé závažné a spojené s komplikacemi (viz bod 4.8).
Osteonekróza dolní čelisti / čelisti
Osteonekróza čelisti, obvykle spojená s extrakcí zubu a / nebo lokální infekcí (včetně osteomyelitidy), byla hlášena u pacientů s rakovinou, kteří dostávali režimy včetně bisfosfonátů podávaných primárně intravenózně. Mnoho z těchto pacientů bylo také léčeno chemoterapií a kortikosteroidy. Osteonekróza čelisti byla také hlášena u pacientů s osteoporózou léčených perorálními bisfosfonáty.
Při posuzování individuálního rizika vzniku osteonekrózy čelisti je třeba vzít v úvahu následující rizikové faktory:
• účinnost bisfosfonátu (maximum pro kyselinu zoledronovou), způsob podání (viz výše) a kumulativní dávka
• rakovina, chemoterapie, radioterapie, kortikosteroidy, inhibitory angiogeneze, kouření
• anamnéza zubního onemocnění, špatná ústní hygiena, periodontální onemocnění, invazivní zubní zákroky a špatně padnoucí zubní protézy.
Před zahájením léčby perorálními bisfosfonáty u pacientů se špatným zubním zdravím by měla být zvážena potřeba zubního vyšetření s vhodnými preventivními zubními zákroky.
Během léčby by se tito pacienti měli pokud možno vyhýbat invazivním zubním zákrokům. U pacientů, u kterých se během léčby bisfosfonáty vyvinula osteonekróza čelisti, může zubní chirurgie tento stav zhoršit. U pacientů vyžadujících zubní výkony nejsou k dispozici žádné údaje, které by naznačovaly přerušení léčby bisfosfonáty. Bisfosfonáty snižují riziko osteonekrózy čelisti. Klinický úsudek lékaře se musí řídit programem řízení každého pacienta na základě individuálního posouzení poměru rizika a přínosu.
Během léčby bisfosfonáty by měli být všichni pacienti povzbuzováni k udržování dobré ústní hygieny, k pravidelným zubním prohlídkám a hlášení jakéhokoli typu orálních příznaků, jako je pohyblivost zubů, bolest nebo otok.
Osteonekróza zevního zvukovodu
Osteonekróza zevního zvukovodu byla hlášena v souvislosti s použitím bisfosfonátů, převážně ve spojení s dlouhodobými terapiemi.Možné rizikové faktory pro osteonekrózu zevního zvukovodu zahrnují použití steroidů a chemoterapie a / nebo lokální rizikové faktory, jako je jako infekce nebo trauma. Osteonekróza zevního zvukovodu by měla být zvážena u pacientů léčených bisfosfonáty, u nichž se projevují ušní příznaky jako bolest nebo výtok nebo chronické ušní infekce.
Muskuloskeletální bolest
U pacientů užívajících bisfosfonáty byla hlášena bolest kostí, kloubů a / nebo svalů. Po uvedení přípravku na trh byly tyto příznaky zřídka závažné a / nebo způsobily invaliditu (viz bod 4.8). Načasování nástupu symptomů se pohybovalo od jednoho dne do několika měsíců po zahájení léčby.Ukončení léčby vedlo u většiny pacientů ke zmírnění symptomů. Po opakovaném podání stejného léku nebo jiného bisfosfonátu došlo u podskupiny pacientů k relapsu symptomů.
Atypické zlomeniny stehenní kosti
Byly hlášeny atypické subtrochanterické a diafyzární zlomeniny stehenní kosti, zejména u pacientů na dlouhodobé léčbě osteoporózy bisfosfonáty. Tyto krátké příčné nebo šikmé zlomeniny se mohou objevit kdekoli ve stehenní kosti od těsně pod malým trochanterem až nad suprakondylickou linii. dochází spontánně nebo po minimálním traumatu a u některých pacientů se objevují bolesti stehen nebo třísel, často spojené se zobrazovacími známkami stresových zlomenin, týdny nebo měsíce před zlomeninou kyčle. Zlomeniny jsou často oboustranné; proto u pacientů léčených bisfosfonáty, kteří utrpěli zlomeninu stehenní zlomeniny, by měla být vyšetřena kontralaterální femur. Bylo také hlášeno omezené hojení těchto zlomenin. U pacientů s podezřením na atypickou zlomeninu stehenní kosti by mělo být zváženo přerušení léčby bisfosfonáty až do posouzení pacienta na základě individuálního rizika prospěchu.
Během léčby bisfosfonáty by pacienti měli být poučeni, aby hlásili jakoukoli bolest stehna, kyčle nebo třísla a každý pacient, který vykazuje tyto příznaky, by měl být vyšetřen na přítomnost neúplné zlomeniny stehenní kosti.
Porucha funkce ledvin
Použití přípravku ADROVANCE u pacientů s poruchou funkce ledvin se nedoporučuje, pokud je clearance kreatininu nižší než 35 ml / min (viz bod 4.2).
Kostní a minerální metabolismus
Příčiny osteoporózy jiné než nedostatek estrogenu a věk musí být pečlivě zváženy.
Před zahájením léčby přípravkem ADROVANCE je třeba upravit hypokalcemii (viz bod 4.3).Jiné poruchy minerálního metabolismu (jako je nedostatek vitaminu D a hypoparatyreóza) by také měly být adekvátně léčeny před zahájením léčby tímto léčivým přípravkem. Obsah vitaminu D v přípravku ADROVANCE není vhodný k nápravě nedostatku vitaminu D. s těmito klinickými stavy, hladinami vápníku v séru a během léčby přípravkem ADROVANCE je třeba sledovat příznaky hypokalcemie.
Vzhledem k pozitivnímu účinku alendronátu na zvýšenou mineralizaci kostí může dojít ke snížení hladin vápníku a fosfátů v séru, zejména u pacientů užívajících glukokortikoidy, u kterých může být absorpce vápníku snížena.Takovýto pokles je obvykle vzácný. závažné a často u pacientů s predisponujícími stavy (např. hypoparatyreóza, nedostatek vitaminu D a malabsorpce vápníku) (viz bod 4.8).
Cholekalciferol
Vitamin D3 může zvýšit rozsah hyperkalcémie a / nebo hyperkalciurie, pokud je podáván pacientům s chorobami spojenými s nepravidelnou nadprodukcí kalcitriolu (např. Leukémie, lymfom, sarkoidóza). U těchto pacientů by mělo být monitorováno sérové a sérové kalcium.
Pacienti s malabsorpcí nemusí dostatečně absorbovat vitamín D3.
Pomocné látky
Tento léčivý přípravek obsahuje laktózu a sacharózu. Pacienti se vzácnými dědičnými problémy s intolerancí fruktózy, intolerancí galaktózy, vrozeným deficitem laktázy, malabsorpcí glukózo-galaktózy nebo nedostatečností sacharázy a izomaltázy by tento přípravek neměli užívat.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Alendronát
Potraviny a nápoje (včetně minerální vody), doplňky vápníku, antacida a další orální léky, pokud jsou užívány současně s alendronátem, pravděpodobně interferují s absorpcí alendronátu. V důsledku toho by pacienti měli nechat uplynout nejméně 30 minut po užití alendronátu, než začnou užívat jakýkoli jiný léčivý přípravek perorálně (viz body 4.2 a 5.2).
Protože užívání nesteroidních protizánětlivých léků (NSAID) je spojeno s podrážděním gastrointestinálního traktu, je při souběžné léčbě alendronátem nutná opatrnost.
Cholekalciferol
Olestra, minerální oleje, orlistat a látky sekvestrující žluč (např. Cholestyramin, colestipol) mohou bránit absorpci vitaminu D. Antikonvulziva, cimetidin a thiazidy mohou zvýšit katabolismus vitaminu D. Další doplňky vitaminu D lze zvažovat individuálně .
04.6 Těhotenství a kojení
ADROVANCE je určen pouze pro ženy po menopauze, a proto by neměl být používán během těhotenství nebo kojení.
Těhotenství
Neexistují žádné nebo omezené údaje o použití alendronátu u těhotných žen. Studie na zvířatech prokázaly reprodukční toxicitu. Alendronát způsoboval dystokii v důsledku hypokalcemie u březích potkanů (viz bod 5.3) Při vysokých dávkách vitaminu D byla pozorována hyperkalcémie a reprodukční toxicita ve studiích na zvířatech (viz bod 5.3) ADROVANCE by neměl být používán během březosti.
Čas krmení
Není známo, zda se alendronát / metabolity vylučují do lidského mléka. Nelze vyloučit riziko pro novorozence / kojence. Cholekalciferol a některé jeho aktivní metabolity přecházejí do mateřského mléka. ADROVANCE by neměl být používán během kojení.
Plodnost
Bisfosfonáty jsou začleněny do kostní matrice, ze které se postupně uvolňují po dobu let. Množství bisfosfonátů začleněných do dospělé kosti, a tedy množství dostupné pro uvolňování do systémového oběhu, přímo souvisí s dávkou a délkou užívání bisfosfonátu (viz bod 5.2). Neexistují žádné údaje o rizikovém účinku na plod u člověka. Pokud však žena po absolvování léčby bisfosfonáty otěhotní, existuje teoretické riziko poškození plodu, zejména kosterního. Vliv na riziko proměnných, jako je doba od ukončení léčby bisfosfonáty do početí, typ použitého bisfosfonátu a způsob podání (intravenózní versus orální) nebyl studován.
04.7 Účinky na schopnost řídit a obsluhovat stroje
ADROVANCE nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje. U pacientů se mohou objevit některé nežádoucí účinky (např. Rozmazané vidění, závratě a silné bolesti kostí, svalů nebo kloubů (viz bod 4.8)), které mohou ovlivnit schopnost řídit a obsluhovat stroje.
04.8 Nežádoucí účinky
Shrnutí bezpečnostního profilu
Nejčastěji hlášenými nežádoucími účinky jsou nežádoucí účinky v horní části gastrointestinálního traktu včetně bolesti břicha, dyspepsie, jícnového vředu, dysfagie, distenze břicha a regurgitace kyseliny (> 1%).
Tabulka nežádoucích účinků
Následující nežádoucí účinky pocházejí z klinických studií a / nebo z používání alendronátu po jeho uvedení na trh.
Při kombinaci alendronátu a cholekalciferolu nebyly identifikovány žádné další nežádoucí účinky.
Frekvence jsou definovány jako: velmi časté (≥ 1/10), časté (≥ 1/100 až
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky, které se vyskytnou po registraci léčivého přípravku, je důležité, protože umožňuje průběžné sledování poměru přínosu a rizika léčivého přípravku. Zdravotničtí pracovníci jsou požádáni, aby hlásili jakékoli podezření na nežádoucí účinky prostřednictvím italské agentury pro léčivé přípravky. , webové stránky: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Předávkování
Alendronát
Příznaky
Hypokalcemie, hypofosfatemie a nežádoucí účinky v horní části gastrointestinálního traktu, jako jsou žaludeční poruchy, pálení žáhy, ezofagitida, gastritida nebo vřed, mohou být důsledkem předávkování ústy.
Řízení
Nejsou k dispozici žádné konkrétní informace o léčbě předávkování alendronátem. V případě předávkování přípravkem ADROVANCE podávejte mléko nebo antacida, která se váží na alendronát.Vzhledem k riziku podráždění jícnu nevyvolávejte zvracení a udržujte pacienta přísně vzpřímený.
Cholekalciferol
Toxicita vitaminu D nebyla během chronické léčby dokumentována u obecně zdravých dospělých v dávce nižší než 10 000 IU / den. V klinické studii u zdravých dospělých nebyla denní dávka 4 000 IU vitaminu D3 po dobu až pěti měsíců spojena s hyperkalciurií nebo hyperkalcémií.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: léčiva k léčbě onemocnění kostí, bisfosfonáty, kombinace.
ATC kód: M05BB03.
Mechanismus účinku
Alendronát
Alendronát sodný je bisfosfonát, který působí jako specifický inhibitor osteoklastem zprostředkované kostní resorpce bez přímého vlivu na tvorbu kosti.Předklinické studie ukázaly, že alendronát se přednostně lokalizuje do míst aktivní resorpce. Aktivita je inhibována, ale nábor a adheze osteoklastů nejsou ovlivněny. Kostní tkáň vytvořená během léčby alendronátem je kvalitativně normální.
Cholekalciferol (vitamín D3)
Vitamín D3 se vyrábí v kůži přeměnou 7-dehydrocholesterolu na vitamín D3 ultrafialovým světlem. Při absenci adekvátního vystavení slunečnímu záření je vitamin D3 nezbytnou živinou. Vitamín D3 se v játrech přeměňuje na 25-hydroxyvitamin D3 a ukládá se pro potřeby těla. Konverze v ledvinách na 1,25-dihydroxyvitamin D3 (kalcitriol), aktivní forma hormonu, který mobilizuje vápník, je podroben pečlivé nastavení. Hlavní aktivitou 1,25-dihydroxyvitaminu D3 je zvýšení absorpce vápníku i fosfátu ve střevě a regulace sérového vápníku, renální vylučování vápníku a fosfátu, tvorba kosti a kostní resorpce.
Vitamín D3 je potřebný pro normální tvorbu kostí. Nedostatek vitaminu D nastává, když je nedostatečné jak vystavení slunečnímu záření, tak dietní příjem. Nedostatek je spojen s negativní bilancí vápníku, ztrátou kostní hmoty a zvýšeným rizikem zlomenin skeletu. V závažných případech má nedostatek za následek sekundární hyperparatyreózu, hypofosfatemii, slabost proximálních svalů a osteomalaci, čímž se zvyšuje riziko pádů a zlomenin u lidí s osteoporózou Doplňky vitaminu D tato rizika a jejich důsledky snižují.
Osteoporóza je definována jako kostní minerální denzita (BMD) páteře nebo kyčle, která je o 2,5 směrodatných odchylek (SD) nižší než průměrná hodnota normální mladé populace, nebo jako anamnéza zlomeniny křehkosti, bez ohledu na BMD.
Klinická účinnost a bezpečnost
Studie ADROVANCE
Účinek nižší dávky přípravku ADROVANCE (alendronát 70 mg / vitamín D3 2 800 IU) na parametry vitaminu D byl prokázán v 15týdenní nadnárodní studii zahrnující 682 postmenopauzálních žen s osteoporózou (25- Výchozí sérové množství hydroxyvitaminu D: průměr 56 nmol / l [22,3 ng / ml]; rozmezí 22,5-225 nmol / l [9-90 ng / ml]). Pacienti byli léčeni přípravkem ADROVANCE (70 mg / 2800 IU) s nižší dávkou (n = 350) nebo FOSAMAX ( alendronát) 70 mg (n = 332) jednou týdně; další doplňky vitaminu D byly zakázány. Sérum 25-hydroxyvitamin D bylo významně vyšší (26%) ve skupině ADROVANCE (70 mg / 2 800 IU) (56 nmol / l [23 ng / ml]) ve srovnání se skupinou léčenou samotným alendronátem (46 nmol / l [18, 2 ng / ml]). Procento pacientů s nedostatečností vitaminu D (sérum 25-hydroxyvitamin D
Ve 24týdenní prodloužené studii zahrnující 619 postmenopauzálních žen s osteoporózou byl prokázán účinek nižší dávky přípravku ADROVANCE (alendronát 70 mg / vitamín D3 2 800 IU) plus 2 800 dalších IU vitaminu D3. Na celkem 5 600 IU (odpovídající na množství vitaminu D3 v nejvyšší dávce ADROVANCE) jednou týdně.Pacienti ve skupině vitaminu D3 2800 byli léčeni přípravkem ADROVANCE (70 mg / 2800 IU) (n = 299) a pacienti ve skupině vitaminu D3 5600 byli léčeni ADROVANCE (70 mg / 2 800 IU) plus dalších 2 800 IU vitaminu D3 (n = 309) jednou týdně; bylo povoleno použití dalších doplňků vitaminu D. Po 24 týdnech léčby byly průměrné sérové hladiny 25-hydroxyvitaminu D významně vyšší v skupina vitaminu D3 5 600 (69 nmol / l [27,6 ng / ml]) ve srovnání s vitamínem D3 2 800 (64 nmol / l [25, 5 ng / ml]). Procento pacientů s nedostatečností vitaminu D bylo 5,4% ve skupině s vitamínem D3 2 800 vs. 3,2% ve skupině vitaminu D3 5600 po dobu prodloužení na 24 týdnů. Procento pacientů s nedostatkem vitaminu D bylo 0,3% ve skupině vitaminu D3 2800 vs nulové ve skupině vitaminu D 35600. byly rozdíly v průměrném sérovém vápníku a fosfátu hladiny nebo 24hodinový močový vápník mezi léčebnými skupinami. Procento pacientů s hyperkalciurií na konci 24týdenního prodlouženého období nebylo mezi léčebnými skupinami statisticky odlišné.
Studie o alendronátu
Terapeutická ekvivalence alendronátu 70 mg jednou týdně (n = 519) a alendronátu 10 mg / den (n = 370) byla prokázána v roční multicentrické studii postmenopauzálních žen s osteoporózou.Průměrné zvýšení BMD lumbální páteře oproti výchozím hodnotám za jeden rok bylo 5,1% (95% interval spolehlivosti -IC- 4,8, 5,4%) ve skupině s dávkou 70 mg jednou týdně. Týdně a 5,4% (95% CI: 5,0, 5,8%) v skupina 10 mg / den. Průměrné zvýšení BMD bylo 2,3% a 2,9% v oblasti krčku stehenní kosti a 2,9% a 3,1% v oblasti kyčle u skupin 70 mg, v uvedeném pořadí. Jednou týdně a 10 mg jednou denně Obě léčebné skupiny byly také podobné, pokud jde o zvýšení BMD v jiných kostních oblastech.
Účinky alendronátu na kostní hmotu a výskyt zlomenin u postmenopauzálních žen byly zkoumány ve dvou počátečních studiích účinnosti stejného designu (n = 994) a ve studii Fracture Intervention Trial (FIT: n = 6 459).).
V počátečních studiích účinnosti bylo průměrné zvýšení BMD s alendronátem 10 mg / den ve srovnání s placebem po dobu tří let 8,8%, 5,9%a 7,8%v oblasti páteře, páteře, krčku stehenní kosti a trochanteru. Také DMO organismu in toto výrazně se zvýšil. C "bylo snížení o 48% (alendronát 3,2% vs placebo 6,2%) v poměru pacientů léčených alendronátem s jednou nebo více zlomeninami obratlů ve srovnání s pacienty léčenými placebem. Ve dvouletém prodloužení těchto studií se BMD nadále zvyšovala v páteři a trochanteru a zůstala stabilní v oblasti krčku a těla stehenní kosti. in toto.
FIT se skládá ze dvou placebem kontrolovaných studií s alendronátem jednou denně (5 mg denně po dobu dvou let a 10 mg denně po dobu jednoho nebo dvou dalších let):
• FIT 1: Tříletá studie s 2 027 pacienty s alespoň jednou zlomeninou obratle (kompresí) na počátku. V této studii denní příjem alendronátu snížil výskyt ≥ 1 nové zlomeniny obratle o 47% (alendronát 7,9% vs placebo 15,0%). Došlo také ke statisticky významnému snížení výskytu zlomenin kyčle (1,1% vs 2,2%, snížení o 51%).
• FIT 2: Čtyřletá studie 4 432 pacientů s nízkou kostní hmotou, ale bez zlomenin obratlů na počátku. V této studii byl pozorován významný rozdíl v podskupinové analýze osteoporotických žen (37% celosvětové populace studie s osteoporózou, jak je definována výše) ve výskytu zlomenin kyčle (alendronát 1,0% vs placebo 2,2%, snížení o 56%) a ve výskytu ≥ 1 zlomeniny obratle (2,9% vs 5,8%, snížení o 50%).
Laboratorní údaje
V klinických studiích byly asymptomatické, mírné a přechodné poklesy sérového vápníku a fosfátu hlášeny u přibližně 18% respektive 10% pacientů léčených alendronátem 10 mg / den, ve srovnání s přibližně 12% a 3% pacientů léčených placebem. . Výskyt sérového vápníku však klesá až
Pediatrická populace
Alendronát sodný byl studován na malém počtu pacientů mladších 18 let s osteogenesis imperfecta. Výsledky nejsou dostatečné pro podporu použití alendronátu sodného u pediatrických pacientů s osteogenesis imperfecta.
05.2 Farmakokinetické vlastnosti
Alendronát
Vstřebávání
Ve srovnání s intravenózní referenční dávkou byla průměrná orální biologická dostupnost alendronátu u žen 0,64% u dávek v rozmezí od 5 mg do 70 mg podávaných po nočním půstu a 2 hodiny před standardizovanou snídaní. Podobně se biologická dostupnost snížila na přibližně 0,46% a 0,39 %, když byl alendronát podáván „hodinu nebo půl“ před standardizovanou snídaní. Ve studiích osteoporózy byl alendronát účinný, pokud byl podán nejméně 30 minut před prvním jídlem nebo nápojem dne.
Alendronát obsažený v kombinované tabletě ADROVANCE (70 mg / 2 800 IU) a kombinované tabletě ADROVANCE (70 mg / 5 600 IU) je bioekvivalentní jedné alendronátové 70 mg tabletě.
Biologická dostupnost byla zanedbatelná, pokud byl alendronát podáván se standardizovanou snídaní nebo do dvou hodin od ní. Souběžné podávání kávy nebo pomerančového džusu s alendronátem snížilo její biologickou dostupnost přibližně o 60%.
U zdravých subjektů prednison podávaný perorálně (20 mg třikrát denně po dobu pěti dnů) nevyvolával klinicky relevantní změny v orální biologické dostupnosti alendronátu (průměrné zvýšení o 20% až 44%).
Rozdělení
Studie na potkanech ukazují, že po intravenózním podání 1 mg / kg l "alendronátu, původně distribuovaného v měkkých tkáních, se rychle redistribuuje do kosti nebo se vylučuje močí. U lidí je průměrný distribuční objem v ustáleném stavu, bez kosti, je nejméně 28 litrů. Plazmatické koncentrace alendronátu po terapeutických perorálních dávkách jsou příliš nízké na to, aby je bylo možné analyticky detekovat (plazmatický protein je přibližně 78%.
Biotransformace
U lidí i zvířat neexistuje důkaz, že je alendronát metabolizován.
Odstranění
Po jednorázové intravenózní dávce alendronátu značeného 14C bylo přibližně 50% radioaktivity vyloučeno do moči během 72 hodin a ve stolici byla získána malá nebo žádná radioaktivita. Po jednorázovém intravenózním podání 10 mg se odbavení ledviny alendronátu byly 71 ml / min odbavení systémové nepřekročilo 200 ml / min. Plazmatické koncentrace klesly o více než 95% během 6 hodin po intravenózním podání. Odhaduje se, že konečný poločas u lidí přesahuje deset let, což odráží uvolňování alendronátu z kostry. „Člověk na této úrovni zasahuje do vylučování jiných léků“.
Cholekalciferol
Vstřebávání
U zdravých dospělých (obou pohlaví) po podání tablet ADROVANCE 70 mg / 2800 IU ráno nalačno a dvě hodiny před jídlem je průměrná plocha pod křivkou koncentrace v čase v séru (AUC0-120 h) pro vitamín D3 (neupraveno na endogenní hladiny vitaminu D3) bylo 296,4 ng • h / ml. Průměrná maximální sérová koncentrace (Cmax) vitaminu D3 byla 5,9 ng / ml a medián času potřebný k dosažení maximální sérové koncentrace (Tmax) byl 12 hodiny Biologická dostupnost 2 800 IU vitaminu D3 v přípravku ADROVANCE je podobná jako 2 800 IU vitaminu D3 podávaného samostatně.
U zdravých dospělých (obou pohlaví) byla po podání tablet ADROVANCE 70 mg / 5 600 IU ráno nalačno a dvě hodiny před jídlem průměrná plocha pod křivkou koncentrace v séru a časem (AUC0-80 h) pro vitamin D3 (neupravený na endogenní hladiny vitaminu D3) byl 490,2 ng • h / ml. Průměrná maximální sérová koncentrace (Cmax) vitaminu D3 byla 12,2 ng / ml a časový medián potřebný k dosažení maximální sérové koncentrace (Tmax) byl 10,6 hodiny Biologická dostupnost 5 600 IU vitaminu D3 v přípravku ADROVANCE je podobná jako 5 600 IU vitaminu D3 podávaného samostatně.
Rozdělení
Po absorpci se vitamín D3 dostává do krevního oběhu přenášeného chylomikrony. Vitamín D3 se rychle distribuuje převážně v játrech, kde se metabolizuje na 25-hydroxyvitamin D3, hlavní rezervní formu. Zanedbatelnější množství se distribuuje do tukových tkání. A svalů a uchovává se tato místa jako vitamín D3 pro pozdější uvolňování do oběhu. Cirkulující vitamín D3 je vázán na protein vázající vitamín D.
Biotransformace
Vitamín D3 je rychle metabolizován hydroxylací v játrech na 25-hydroxyvitamin D3 a následně metabolizován v ledvinách na 1,25-dihydroxyvitamin D3, což je biologicky aktivní forma. Další hydroxylace probíhá před eliminací. Malé procento vitaminu D3 podléhá před vyloučením glukuronidaci.
Odstranění
Při podávání radioaktivního vitaminu D3 zdravým lidem bylo průměrné vylučování radioaktivity močí po 48 hodinách 2,4%a průměrné vylučování radioaktivity stolicí po 4 dnech 4,9%. V obou případech bylo zjištěno, že vyloučená radioaktivita pochází téměř výhradně z metabolitů původní molekuly. Průměrný poločas sérového vitaminu D3 po perorální dávce přípravku ADROVANCE (70 mg / 2 800 IU) je přibližně 24 hodin.
Porucha funkce ledvin
Předklinické studie ukazují, že alendronát, který se neusazuje v kostech, se rychle vylučuje močí. Po chronickém podávání kumulativních intravenózních dávek až do 35 mg / kg u zvířat nebyly prokázány saturace vychytávání kostí.
Ačkoli nejsou k dispozici žádné klinické informace, je pravděpodobné, že stejně jako u zvířat bude renální eliminace alendronátu u pacientů s poruchou funkce ledvin snížena. V důsledku toho lze u pacientů s poruchou funkce ledvin očekávat mírně vyšší akumulaci alendronátu v kosti ( viz bod 4.2).
05.3 Předklinické údaje vztahující se k bezpečnosti
Neklinické studie nebyly provedeny s kombinací alendronátu a cholekalciferolu.
Alendronát
Neklinické údaje na základě konvenčních studií neodhalily žádné zvláštní riziko pro člověka farmakologie bezpečnosti, toxicita po opakovaných dávkách, genotoxicita a karcinogenní potenciál. Studie na potkanech ukázaly, že léčba alendronátem během těhotenství je spojena s dystokií spojenou s hypokalcemií u matek během porodu. Ve studiích vykazovaly potkany, kterým byly podány nejvyšší dávky, vyšší výskyt neúplné osifikace plodu. Relevance těchto nálezů pro člověka není známa.
Cholekalciferol
Při dávkách vysoko nad terapeutickým rozsahem byla ve studiích na zvířatech pozorována reprodukční toxicita.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Mikrokrystalická celulóza (E460)
Bezvodá laktóza
Triglyceridy se středním řetězcem
Želé
Sodná sůl kroskarmelózy
Sacharóza
Koloidní oxid křemičitý
Stearát hořečnatý (E572)
Butylovaný hydroxytoluen (E321)
Upravený škrob (kukuřice)
Křemičitan sodný (E554)
06.2 Neslučitelnost
Irelevantní.
06.3 Doba platnosti
18 měsíců.
06.4 Zvláštní opatření pro skladování
Uchovávejte v původním blistru, aby byl přípravek chráněn před vlhkostí a světlem.
06.5 Charakter vnitřního obalu a obsah balení
ADROVANCE 70 mg / 2 800 IU tablety
Al / Al blistry v balení po 2, 4, 6 nebo 12 tabletách.
ADROVANCE 70 mg / 5 600 IU tablety
Al / Al blistry v balení po 2, 4 nebo 12 tabletách.
Na trhu nemusí být všechny velikosti balení.
06.6 Návod k použití a zacházení
Žádné zvláštní pokyny.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Merck Sharp & Dohme Ltd.
Hertford Road, Hoddesdon
Hertfordshire EN11 9BU
Spojené království
08.0 REGISTRAČNÍ ČÍSLO
ADROVANCE 70 mg / 2 800 IU tablety
EU/1/06/364/001 - 2 tablety
037603014
EU/1/06/364/002 - 4 tablety
037603026
EU/1/06/364/003 - 6 tablet
037603038
EU/1/06/364/004 - 12 tablet
037603040
ADROVANCE 70 mg / 5 600 IU tablety
EU/1/06/364/006 - 2 tablety
037603065
EU/1/06/364/007 - 4 tablety
037603077
EU/1/06/364/008 - 12 tablet
037603089
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Datum první registrace: 4. ledna 2007
Datum posledního obnovení: 21. listopadu 2011
10.0 DATUM REVIZE TEXTU
19. září 2016