Všeobecnost
Léčba chronické myeloidní leukémie (CML) zahrnuje několik terapeutických možností, které mohou udržet onemocnění pod kontrolou po delší dobu. Rutinní testy krve a kostní dřeně a časté hodnocení hematologem nebo onkologem mohou sledovat progresi rakoviny.

Z výsledků lékařských vyšetření (krevní obraz, cytogenetické a molekulární testy) lze pochopit:
- Stupeň účinnosti léčby v průběhu času a vývoj reakce na terapii;
- Pokud nemoc již nereaguje na léky (odolnost vůči terapii).
Monitorování a reakce na terapii
Správné sledování průběhu onemocnění je zásadní pro ověření účinnosti terapie a v důsledku toho pro možnost rychlé intervence v případě selhání léčby.
Cytogenetická analýza a vyšetřování molekulární biologie se používají, stejně jako pro diagnostické účely, také k hodnocení stupně odpovědi na terapeutický protokol a k zdůraznění jakékoli perzistence onemocnění po léčbě (studie minimálního reziduálního onemocnění):
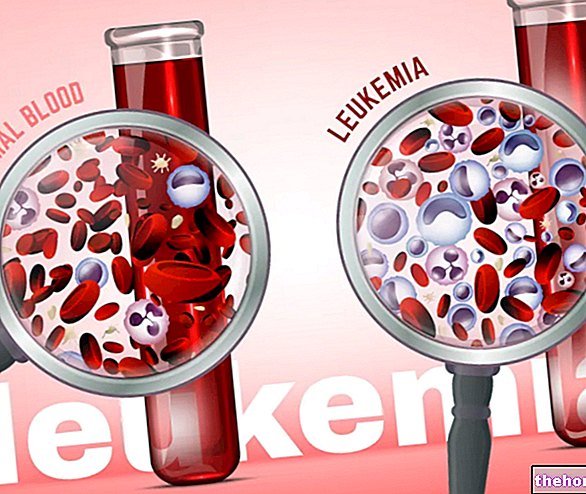
- Kompletní hematologická odpověď: Když terapie začne mít účinek, počet buněk leukémie se sníží. Hematologické testy již nejsou schopny detekovat aberantní klony, ale je to možné pomocí cytogenetické analýzy.
- Kompletní cytogenetická odpověď: získá se, když přítomnost chromozomu Philadelphia (Ph) již není zvýrazněna konvenční cytogenetickou analýzou (standardní přístup ke sledování reakce na léčbu) nebo fluorescenční in situ hybridizací (FISH), technikou, která vyhodnocuje procento Buňky kostní dřeně Ph +. Cytogenetická analýza, provedená na vzorku kostní dřeně odsátého jemnou jehlou, je také jedinou metodou pro stanovení přítomnosti jakýchkoli chromozomálních změn, doplňujících chromozom Philadelphie, s prognostickou rolí.
- Kompletní molekulární odpověď: je dosažena, když molekulární analýza není schopna detekovat expresi hybridního genu BCR / ABL. Terapie se ukázala jako účinná a molekulární signály, které podporují produkci proteinů bcr-abl, jsou tak nízké, že je nelze detekovat ani pomocí vysoce citlivých testů, jako jsou molekulární. Zvýšené hladiny transkriptu, které jsou monitorovány, mohou naznačovat ztrátu odpovědi na léčbu.
Dosažení těchto výsledků představuje velmi důležitý výsledek: mnoho studií ukazuje, že pacienti s kompletní cytogenetickou a molekulární odpovědí mají velmi vysokou pravděpodobnost dlouhodobého přežití bez progrese onemocnění do akcelerované a / nebo blastové fáze. .
Účinnost terapie může ovlivnit mnoho faktorů, a proto se v počátečních fázích doporučuje pokračovat v testech po 3, 6, 12 a 18 měsících.
Dosud získané informace z klinických studií, které definují optimální odpověď a selhání v různých dobách terapie, vedly k formulaci monitorovacího schématu, které je nutné dodržovat pro správnou péči o pacienta (indikace navržené European Leukemia-Net):
Hematolog (nebo onkolog) bude schopen stanovit některé cíle a ověřit účinnost terapie v konkrétním klinickém případě, protože pacienti reagují na terapii odlišně a ne všichni jsou schopni dosáhnout optimálních terapeutických milníků v předpokládaném časovém období ...
Terapeutické možnosti
Hlavním cílem léčby CML je „dosáhnout úplné molekulární remise: nemoc je léčbou kontrolována (i když úplně nezmizí) a počet produkovaných patologických klonů je dostatečně omezen, aby nevyvolával žádné příznaky. Většina lidí nemůže zbavit se buněk leukémie úplně, léčba může pomoci dosáhnout dlouhodobého ústupu nemoci.
Terapeutické cíle mohou zahrnovat:
- Omezit projevy chronické myeloidní leukémie;
- Obnovte normální parametry týkající se počtu krvinek;
- Snižte počet Philadelphia chromozom pozitivních leukemických buněk (Ph +) a molekulárních signálů (transkripty BCR / ABL);
- Cílem je zmizení chromozomů Philadelphia + (úplná cytogenetická odpověď).
Konvenční antiblastická léčiva
Některá antibiotická léčiva, jako např busulfan (alkylační) a l "hydroxymočovina (specifický inhibitor syntézy DNA), byly použity, zejména v minulosti, k dosažení cytoredukce a kontroly onemocnění v chronické fázi. Konvenční léčba vedla ke zlepšení kvality života, ale nebyla schopna významně změnit přirozenou historii onemocnění ani zabránit progresi do zrychlené / blastické fáze.
Rekombinantní interferon-alfa
Od začátku 80. let 20. století bylo zavedeno interferony umožnilo kromě redukce a normalizace podílu granulocytů pozorovat dosažení negativizace cytogenetických a molekulárních testů, navození delšího trvání chronické fáze s následným snížením vývoje ve zrychlené a / nebo blastické fázi. Interferon -alfa omezil úlohu konvenční terapie CML: tento lék je schopen indukovat úplnou cytogenetickou odpověď u 20-30% pacientů, konkrétně interferuje s translací proliferativních signálů v buňkách Ph + a inhibuje progenitory nádorových multiplikací. Interferon-alfa také působí nepřímým mechanismem na přežití buněk leukémie, snižuje jejich buněčnou adhezi a zesiluje aktivitu buněk imunitního systému.
Omezení používání tohoto léčiva je dáno jeho nezanedbatelnou toxicitou. Mezi vedlejší účinky interferonu patří únava, horečka a hubnutí. Za účelem zlepšení dosažených výsledků byl interferon kombinován s jinými cytotoxickými činidly.Ukázalo se, že pouze spojení interferonu s cytosin arabinosidem (ARA-C) nabízí lepší výsledky než samotný interferon, bez zjevné výhody přežití.
Alogenní transplantace kostní dřeně
Transplantace kmenových buněk od zdravého dárce kompatibilního s příjemcem (alogenní transplantace) představuje již léta nejčastější terapeutickou indikaci a dodnes představuje jedinou léčbu, která je schopná novotvar definitivně vymýtit.
Tento postup, pokud je prováděn v chronické fázi, může mít za následek přibližně pětileté přežití bez onemocnění v přibližně 50% případů.
Alogenní transplantace kostní dřeně zahrnuje první fázi destrukce všech (nebo téměř všech) buněk Ph + pomocí kondiční terapie (chemoterapie v kombinaci s ozařováním celého těla), po níž následuje rekonstituce hematopoetické dřeně infundovanými kmenovými buňkami dárce. Lymfocyty dárcovské dřeně navíc přispívají ke kontrole a / nebo eliminaci jakýchkoli buněk Ph + s imunitně zprostředkovaným efektem, který se nazývá efekt „štěp proti leukémii“ (štěp proti leukémii). Odpověď na terapii lze monitorovat zhodnocením, zda molekulární změny typické pro chronickou myeloidní leukémii vymizely či nikoli. Alogenní transplantace kostní dřeně představuje terapeutickou léčbu schopnou „vyléčit“ CML, ale bohužel zahrnuje míru selhání v důsledku smrtelné toxicity a / nebo relapsu. Tento postup je ve skutečnosti velmi náročný a může být ovlivněn věkem pacient. pacient a předčasnost transplantace (měsíce nebo roky od diagnózy chronické fáze): vzhledem k potenciálnímu nebezpečí je proveditelný pouze u pacientů mladších 55 let bez dalších souběžných patologií. Alogenní transplantace proto představuje skutečnou terapeutickou příležitost pouze pro menšinu pacientů s CML (také s ohledem na obtíže při hledání kompatibilního dárce kmenových buněk).
Nedávno byla u subjektů s chronickou myeloidní leukémií, které nejsou způsobilé k aloštěpu (věk, nedostatek dárce, odmítnutí atd.), Navržena autotransplantace. Kostní dřeň pacienta, reinfúzovaná po „záměrně adekvátní cytocidní terapii pro Ph + buňky (s antiblastickým + interferonem), by se sama rekonstituovala s převládající re-expanzí Ph-buněk.
Imatinib mesylát (Glivec ®)
Historie léčby chronické myeloidní leukémie byla revolucí díky zavedení prvního inhibitoru tyrosinkinázy (Imatinib mesylate), který významně přispěl ke zlepšení kvality života pacientů.
Imatinib je specifický inhibitor BCR / ABL, navržený po porozumění molekulární biologii onemocnění a používaný při léčbě Ph + chronické myeloidní leukémie.
Lék je schopen vyvolat úplnou molekulární cytogenetickou remisi u 80-90% pacientů a je také aktivní u myeloidních novotvarů s eozinofilií a postižením PDGRF (destičkový růstový faktor, sérový mitogen zapojený do mnoha patologických stavů, který podporuje chemotaxi a proliferativní kapacita).
Imatinib selektivně blokuje aktivitu tyrosinkinázy BCR / ABL prostřednictvím inhibičního mechanismu ATP: léčivo váže vysokou energetickou molekulu (ATP) dostupnou ve specifické doméně BCR / ABL kinázy, čímž brání fosforylaci jiných substrátů a blokuje kaskádu reakcí, které by byly zodpovědné za proces generování Ph + leukemických klonů. Použitá dávka této molekuly (imatinib methysilátu) se pohybuje od 400 mg / den do 800 mg / den ve vztahu k fázi onemocnění a odpovědi. V současné době je díky své pozoruhodné účinnosti lékem první volby pro léčbu CML. Vedlejší účinky, reverzibilní se suspenzí a / nebo snížením dávky, mohou být různé (zvýšené transaminázy, nevolnost, kožní vyrážky, zadržování tekutin atd.).
Byly pozorovány případy vykazující rezistenci na léčivo v průběhu času (například pacienti s pokročilým onemocněním) a byla identifikována biologicko-klinická kritéria pro definování typu odpovědi na léčbu. Mechanismy odpovědné za tuto rezistenci se zdají být mnohočetné (mutace kinázové domény, amplifikace / nadměrná exprese BCR / ABL, klonální evoluce ...). V těchto případech již není pokračování léčby Imatinibem vhodné.
U pacientů s těmito stavy jsou možné možnosti:
- Alogenní transplantace;
- Konvenční terapie (hydroxymočovina, busulfan atd.);
- L "interferon;
- Experimentální terapie (s inhibitory tyrosinkinázy 2. generace).
Inhibitory tyrosinkinázy 2. generace
Selhání léčby imatinibem je spojeno s progresí chronické myeloidní leukémie ve zrychlené a / nebo blastické fázi a má zvláště špatnou prognózu. V posledních letech umožnil farmakologický výzkum v klinické praxi použití inhibitorů tyrosinkinázy druhé generace, aktivních u pacientů, u kterých se vyvinula rezistence na Imatinib: Dasatinib (Sprycel®) a Nilotinib (Tasigna®) se používají u pacientů s chronickou fází a / nebo progresivní CML refrakterní na Glivec ® a jsou schopné znovu indukovat úplné a trvalé hematologické, cytogenetické a molekulární reakce.Četné studie však ukázaly, že klon Ph + - díky své genetické nestabilitě - může vyvinout mutace doménu BCR / ABL kinázy a prokázat odolnost vůči různým inhibičním léčivům. Jiné molekuly v experimentální fázi (inhibitory 3. generace) jsou zaměřeny na specifické cíle chronické myeloidní leukémie; zejména jsou schopné senzibilizovat leukemické buňky Ph + se specifickými mutacemi (příklad: Mk-0457 pro rezistentní CML a s mutací T315I, která přímo ovlivňuje t vazebné místo imatinibu).
Další články o "Terapii chronické myeloidní leukémie"
- Chronická myeloidní leukémie: Chronická myeloidní leukémie: Diagnóza
- Chronická myeloidní leukémie: Definice, příčiny, příznaky