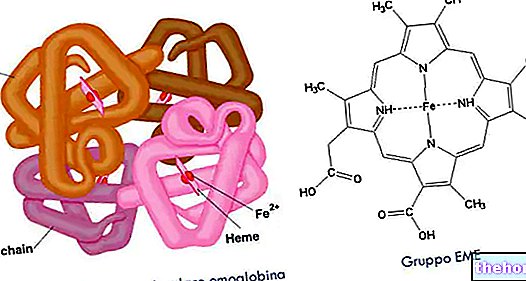
Všeobecnost
Co je aterom?
Aterom, lépe známý jako aterosklerotický plak, lze definovat jako degeneraci arteriálních stěn v důsledku ukládání plaků tvořených v podstatě tukem a jizevnatou tkání.

Komplikace
Tepna naplněná lipidickým materiálem a fibrotickou tkání ztrácí pružnost a odolnost, je náchylnější k prasknutí a zmenšuje svůj vnitřní lumen, což brání průtoku krve. Kromě toho v případě prasknutí ateromu dochází k reparačním a koagulačním procesům, které mohou vést k rychlé okluzi cévy (trombóza), nebo generování více či méně závažných embolií, pokud se fragment ateromu oddělí a je vytlačen - jako zatoulaný důl - na periferii, s rizikem - pokud fibrinolytické jevy nezasáhnou včas - k ucpání dolní arteriální cévy.
Ve světle tohoto popisu je dobře pochopeno, jak aterosklerotické plaky - i když asymptomatické dokonce po celá desetiletí - často způsobují komplikace, typicky od pozdní dospělosti, jako jsou: angina pectoris, infarkt myokardu, mrtvice, gangréna.

Aterom je typickým vyjádřením chronického zánětlivého onemocnění nazývaného ateroskleróza, hlavní příčina kardiovaskulárních onemocnění, která - alespoň v průmyslových zemích - představují hlavní příčinu úmrtí mezi populací.
Struktura arteriálních cév
Většině lidí je známo, že strava bohatá na (nasycené) živočišné tuky a cholesterol - spolu s nadváhou a obezitou, kouřením a sedavým životním stylem - představuje jeden z hlavních rizikových faktorů aterosklerotických onemocnění.
Abychom pochopili, jak vzniká aterom, je nejprve nutné krátce oprášit histologii tepenných stěn, které se skládají ze tří vrstev:
- intimní se svými 150-200 mikrometry v průměru je nejvnitřnější nebo nejhlubší vrstvou cévy, která je v těsném kontaktu s krví; je tvořena převážně endotelovými buňkami, které vymezují lumen cévy tvořící kontakt prvek mezi krví a arteriální stěnou
- střední tunika o průměru 150-350 mikrometrů se skládá z buněk hladkého svalstva, ale také z elastinu (který dodává cévám pružnost) a kolagenu (strukturní složka)
- adventitia představuje nejvzdálenější vrstvu tepny; 300-500 mikrometrů v průměru, obsahuje vláknitou tkáň a je obklopen perivaskulární pojivovou tkání a epikardiálním tukem.
Aterosklerotické léze postihují především velké a střední tepny, kde převládá elastická tkáň (zejména ve velkých tepnách) a svalová tkáň (zejména ve středních a malých tepnách). Kromě toho mají tendenci se vyvíjet v predisponovaných oblastech, jako jsou body rozvětvení tepen charakterizované turbulentním prouděním krve, které šetří sousední segmenty. Aterosklerotický proces začíná velmi brzy, od dospívání (problém obezity dětí) nebo od rané dospělosti.
Biologie ateromu
Aterosklerotický proces začíná z endotelových buněk, poté z nejvnitřnější vrstvy arteriální cévy.
Považovat endoteliální tkáň za jednoduchou výstelku cév je velmi reduktivní, a to natolik, že dnes je endotel považován za skutečný orgán, schopný zpracovat mnoho účinných látek schopných modulovat aktivitu, nejen různých struktur cévní stěny ..., ale také krevních buněk a proteinů koagulačního systému, které přicházejí do styku s povrchem endotelu.Tyto účinné látky se částečně uvolňují v bezprostřední blízkosti (parakrinní sekrece), čímž působí na stěnu cévy, a částečně uvolňují se do krevního oběhu (endokrinní sekrece), aby prováděly své působení na dálku (např. oxid dusnatý a endotelin); další zůstávají přichyceny k povrchu endotelových buněk a provádějí svůj účinek přímým kontaktem, jako se to děje u adheze molekuly pro leukocyty nebo ty, které ovlivňují srážení.
- tepnu nesmíme považovat za jednoduchý kanál, který zaručuje transport krve tam, kde je potřeba. Spíše si ji musíme představit jako dynamický a komplexní orgán složený z různých buněčných a molekulárních aktérů
Stručně řečeno, endotel představuje metabolický základ cévní stěny, až do bodu regulace buněčné proliferace, zánětlivých jevů a trombotických procesů. Z tohoto důvodu hraje endotelová tkáň klíčovou roli v regulaci vstupu, výstupu a metabolismu lipoproteinů a další látky, které se mohou podílet na tvorbě aterosklerotických lézí.
Fáze tvorby a růstu ateromu
Proces vzniku a růstu ateromu, který, jak jsme viděli, se vyvíjí v průběhu let nebo dokonce desetiletí, se skládá z různých fází, které popíšeme níže:
- Adheze, infiltrace a depozice částic LDL lipoproteinu v intimě tepny; toto ložisko má název lipidový pruh („tučný pruh“) a je spojeno hlavně s „přebytkem lipoproteinů LDL (hypercholesterolemie) a / nebo defektem lipoproteinů HDL. Oxidace proteinů LDL hraje hlavní roli v počátečních procesech tvorba ateromu
- Připomínáme, jak oxidaci LDL mohou podpořit volné radikály vytvořené po kouření cigaret (snížená aktivita glutathionperoxidázy), hypertenze (v důsledku zvýšení produkce angiotensinu II), diabetes mellitus (pokročilé produkty glykosylace přítomné u diabetiků), genetické změny a hyperhomocysteinémie; a naopak, reaktivní druhy kyslíku jsou inaktivovány dietními antioxidanty, jako jsou vitamíny C a E, a buněčnými enzymy, jako je glutathionperoxidáza
- Zánětlivý proces spuštěný „zachycením a oxidací LDL lipidů s následným poškozením endotelu vede k expresi adhezních molekul na buněčné membráně a k vylučování biologicky aktivních a chemotaktických látek (cytokiny, růstové faktory, volné radikály) , které společně podporují stažení a následnou infiltraci leukocytů (bílých krvinek) s transformací monocytů na makrofágy;
- připomínáme si, jak oxid dusnatý (NO) produkovaný endotelovými buňkami, kromě svých dobře známých vazodilatačních vlastností, také vykazuje lokální protizánětlivé vlastnosti, omezující expresi adhezních molekul; z tohoto důvodu je v současné době považován za ochranný faktor proti ateroskleróze. Bylo prokázáno, že fyzická aktivita zvyšuje syntézu oxidu dusnatého. V jiných studiích bylo naopak v reakci na akutní tělesné cvičení prokázáno snížení endoteliální adheze leukocytů, přičemž již nějakou dobu je známo, že pravidelné cvičení je spojeno s nižší koncentrací C reaktivního proteinu (teploměr) zánětu) v klidu. Obecněji tělesné cvičení předchází a koriguje určité stavy, které představují riziko aterosklerózy, jako je hypertenze, hyperglykémie a inzulínová rezistence. Kromě toho zvyšuje hladinu HDL a posiluje endogenní antioxidační systémy, čímž brání oxidaci LDL a jejich ukládání v tepnách.
- Makrofágy pohlcují oxidovaný LDL akumulací lipidů v jejich cytoplazmě a přeměnou na pěnové buňky bohaté na cholesterol. Až do tohoto bodu - zatímco představuje (čistě zánětlivou) lézi, která předchází aterosklerotickým plakům - se může lipidový pruh rozpustit. Ve skutečnosti došlo pouze k akumulaci lipidů, volných nebo ve formě pěnivých buněk. V následujících fázích vede akumulace fibrotické tkáně k nevratnému růstu skutečného ateromu.
- Pokud zánětlivá reakce není schopna účinně neutralizovat nebo odstraňovat škodlivé látky, může pokračovat neomezeně dlouho a stimulovat migraci a proliferaci buněk hladkého svalstva, které migrují z tunica media do intimního prostředí, čímž vzniká extracelulární matrix, která funguje jako strukturální lešení aterosklerotický plak (aterom). Pokud tyto reakce pokračují dále, mohou způsobit zesílení arteriální stěny: fibrolipidová léze nahrazuje jednoduchou lipidovou akumulaci počátečních fází a stává se nevratnou. Céva na druhou stranu reaguje procesem nazývané di kompenzační remodelace, snažící se napravit stenózu (zmenšení způsobené plakem), postupně se rozšiřující, aby byl lumen cév nezměněn.
- Syntéza zánětlivých cytokinů endoteliálními buňkami působí jako posilovač imunokompetentních buněk, jako jsou T lymfocyty, monocyty a plazmatické buňky, které migrují z krve a množí se v rámci léze. V tomto okamžiku se věří, že jak léze roste, v důsledku nedostatek živin a hypoxie, buňky hladkého svalstva a makrofágy mohou podstoupit apoptózu (buněčnou smrt), s usazováním vápníku na zbytcích mrtvých buněk a extracelulárních lipidech. Tak vznikají komplikované aterosklerotické léze.
- Konečným výsledkem je tvorba více či méně velké léze, která se skládá z centrálního lipidového jádra (lipidové jádro) obaleného vláknitým pojivovým víčkem (vláknitý uzávěr), infiltrátů imunokompetentních buněk a kalciových uzlin. Je důležité zdůraznit, že v lézích může existovat velká variabilita v histologii vytvořené tkáně: některé aterosklerotické léze vypadají převážně husté a vláknité, jiné mohou obsahovat velké množství lipidů a nekrotických zbytků, zatímco většina přítomných kombinací a variací každá z těchto charakteristik Distribuce lipidů a pojivové tkáně uvnitř lézí určuje jejich stabilitu, snadné lámání a trombózu, s následnými klinickými efekty.
Podívejte se na video
- Podívejte se na video na youtube
Podívejte se na video
- Podívejte se na video na youtube
Příčiny
Výše popsaná patogeneze aterosklerotických plaků ukazuje, jak je ateroskleróza komplexní patologie, na jejímž vzniku se podílejí různé složky cévního, metabolického a imunitního systému.

Nejde tedy o jednoduchou pasivní akumulaci lipidů uvnitř cévní stěny. Jak se však předpokládalo, aterosklerotické plaky mohou uzavřít lumen cévy až o 90%, aniž by vykazovaly klinicky zjevné příznaky. Problémy jsou poměrně závažné. Začínají v rychlý růst krevní sraženiny (trombu) po prasknutí vláknité kapsle nebo endoteliálního povrchu nebo krvácení mikrociev uvnitř léze. Tromby, vytvořené na povrchu nebo uvnitř léze, mohou způsobit akutní příhody dvěma způsoby:
1) mohou se zvětšit in situ, aby se zcela uzavřela céva blokující průtok krve z místa, kde se plak vyvíjí;
2) mohou se oddělit z místa léze a sledovat tok krve, dokud se nezablokují ve větvi malé cévy, což brání toku krve od tohoto bodu dále.
Obě tyto události zabraňují správnému okysličení tkání a vyvolávají jejich nekrózu. Ucpání cévy může být také podporováno vazospasmem indukovaným uvolňováním endotelinu endotelovými buňkami.
Kromě toho může oslabení stěny cévy vést ke generalizované dilataci tepny, což v průběhu let může vést ke vzniku aneuryzmatu.
Abychom to shrnuli, zjednodušení pojmu co nejvíce, tvorba ateromů je důsledkem tří procesů:
- akumulace lipidů, zejména volného cholesterolu a esterů cholesterolu, v subendotelovém prostoru tepen;
- vytvoření zánětlivého stavu s infiltrací lymfocytů a makrofágů, které pohlcením nahromaděných lipidů se stanou pěnovými buňkami;
- migrace a proliferace buněk hladkého svalstva