Co je Lynparza a k čemu se používá?
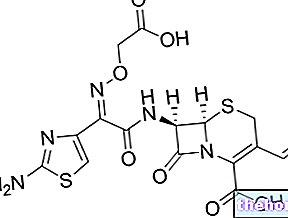
Lynparza je protirakovinový lék určený k `` udržovací`` léčbě dospělých pacientů s vysoce kvalitním serózním epiteliálním karcinomem vaječníků (typ pokročilého stadia rakoviny vaječníků), včetně rakoviny vejcovodů (část reprodukčního systému, která spojuje vaječníky) do dělohy) a karcinom pobřišnice (výstelková membrána břicha). Přípravek Lynparza se používá u pacientů, kteří mají mutace (defekty) v jednom ze dvou genů známých jako BRCA1 a BRCA2 a kteří mají opakující se relapsy (tj. Rakovina se po léčbě vrátí). Přípravek Lynparza se podává po terapii léky na bázi platiny, když se zmenší velikost karcinomu nebo zcela zmizí nádorová hmota. Podává se pacientům, u nichž předchozí léková terapie na bázi platiny vyvolala trvalou odpověď (trvající nejméně 6 měsíců). Lynparza obsahuje léčivou látku olaparib. Protože je počet pacientů s rakovinou vaječníků nízký, je toto onemocnění považováno za `` vzácné`` a Lynparza byla dne 6. prosince 2007 označena za `` léčivý přípravek pro vzácná onemocnění``.
Jak se přípravek Lynparza používá - olaparib?
Lynparza je k dispozici ve formě tobolek (50 mg), které se užívají ústy. Výdej tohoto léčivého přípravku je vázán na lékařský předpis a léčbu by měl zahájit a sledovat lékař, který se specializuje na léčbu rakoviny. Před zahájením terapie si pacienti musí být jisti, že mají genovou mutaci BRCA. Hodnocení stavu mutace by mělo být provedeno ve vhodné laboratoři pomocí genetického testování. Léčba přípravkem Lynparza by měla být zahájena do 8 týdnů od podání poslední dávky chemoterapie na bázi platiny. Doporučená dávka přípravku Lynparza je 400 mg (osm tobolek) podávaných dvakrát denně. Léčbu lze ukončit a dávky lze snížit v případě nežádoucí účinky.
Jak přípravek Lynparza - olaparib funguje?
Léčivá látka v přípravku Lynparza, olaparib, blokuje působení enzymů nazývaných lidská poly (ADP-ribóza) polymeráza (PARP), které pomáhají opravit poškozenou DNA v buňkách (zdravých i rakovinných) během buněčného dělení. Existuje alternativní mechanismus opravy DNA to vyžaduje proteiny BRCA1 a BRCA2. Tento alternativní mechanismus nefunguje správně v rakovinných buňkách, které mají mutace v genu BRCA1 nebo BRCA2. Proto když jsou proteiny PARP blokovány, DNA je v rakovinných buňkách poškozena, nelze ji opravit a jako v důsledku toho rakovinné buňky umírají.
Jaký přínos přípravku Lynparza - olaparib prokázal v průběhu studií?
V jedné hlavní studii zahrnující 265 pacientů s vysoce kvalitním serózním ovariálním karcinomem, včetně karcinomu vejcovodu nebo peritoneálního karcinomu, bylo prokázáno, že přípravek Lynparza prodlužuje dobu, po kterou se u pacientů neprojevuje zhoršení onemocnění. Před posledním léčebným cyklem pacienti podstoupili dva nebo více cyklů chemoterapie na bázi platiny a měli trvalou odpověď (rakovina neprogredovala alespoň 6 měsíců). Tato odpověď na léky na bázi platiny odůvodňovala použití nejnovějších léčba na bázi platiny Lynparza byla podána do 8 týdnů od posledního cyklu chemoterapie na bázi platiny, když byla nádorová hmota v recesi nebo úplně zmizela. Asi polovina pacientů účastnících se studie měla mutace BRCA. Ve většině případů šlo o zděděné mutace. Pacienti s mutací BRCA léčeni přípravkem Lynparza přežili v průměru déle bez známek progrese onemocnění než pacienti s mutací BRCA léčeni placebem (léčbou neúčinným přípravkem), tj. 11,2 měsíce versus 4,3 měsíce.
Jaká rizika jsou spojena s přípravkem Lynparza - olaparib?
Nejčastějšími nežádoucími účinky přípravku Lynparza (které mohou postihnout více než 1 z 10 lidí) jsou únava, nevolnost, zvracení, průjem, dyspepsie (pálení žáhy), bolest hlavy, dysgeuzie (porucha chuti), snížená chuť k jídlu, závratě, anémie (snížení počet červených krvinek), lymfopenie a neutropenie (snížení počtu určitých typů bílých krvinek), zvýšení průměrného korpuskulárního objemu (zvýšení průměrné velikosti červených krvinek) a zvýšení kreatininu (přítomnost hladiny kreatininu indikují problémy s funkcí ledvin.) Úplný seznam všech vedlejších účinků hlášených u přípravku Lynparza je uveden v příbalové informaci. Kojení je během léčby přípravkem Lynparza a nejméně jeden měsíc po poslední dávce kontraindikováno. Úplný seznam omezení naleznete v příbalové informaci.
Na základě čeho byl přípravek Lynparza - olaparib schválen?
Výbor agentury pro humánní léčivé přípravky (CHMP) rozhodl, že přínosy přípravku Lynparza převyšují jeho rizika, a proto doporučil, aby byl schválen k použití v EU. Výbor CHMP je toho názoru, že přínos přípravku Lynparza při prodloužení přežití rakoviny pacienti s mutací BRCA před progresí onemocnění jsou klinicky relevantní. U těchto pacientů, kteří mají obvykle špatnou diagnózu, došlo k celkovému zpoždění progrese onemocnění o 6,9 měsíce, což by mohlo umožnit oddálení dalšího průběhu chemoterapie na bázi platiny z hlediska bezpečnosti byly vedlejší účinky většinou mírné nebo střední a byly obecně zvládnutelné.Výbor CHMP rovněž poznamenal, že jsou zapotřebí další studie, které by dále potvrdily přínos přípravku Lynparza, jeho účinky na celkové přežití a jeho dlouhodobou bezpečnost.
Jaká opatření jsou přijímána k zajištění bezpečného a účinného používání přípravku Lynparza - olaparib?
Byl vyvinut plán řízení rizik, který zajistí, že bude Lynparza používána co nejbezpečněji. Na základě tohoto plánu byly do souhrnu údajů o přípravku a příbalové informace přípravku Lynparza přidány informace o bezpečnosti, včetně příslušných opatření, která by měli zdravotničtí pracovníci a pacienti dodržovat. Kromě toho společnost, která uvádí na trh přípravek Lynparza, provede studie s cílem dále potvrdit přínos tohoto léčivého přípravku, včetně dlouhodobého prospěchu u pacientek s rakovinou vaječníků.
Další informace o přípravku Lynparza - olaparib
Dne 16. prosince 2014 vydala Evropská komise „Registraci“ přípravku Lynparza platnou v celé Evropské unii. Další informace o léčbě přípravkem Lynparza naleznete v příbalové informaci (součástí zprávy EPAR) nebo se poraďte se svým lékařem. Nebo lékárníkem. Shrnutí stanoviska Výboru pro léčivé přípravky pro vzácná onemocnění pro přípravek Lynparza je k dispozici na webových stránkách agentury: ema.Europa.eu/Find medicine / Human medicines / Rare disease identification. Poslední aktualizace tohoto souhrnu: 12-2014.
Informace o službě Lynparza - olaparib zveřejněné na této stránce mohou být zastaralé nebo neúplné. Správné použití těchto informací najdete na stránce Prohlášení a užitečné informace.