Účinné látky: Ipratropium bromid (Ipratropium bromid monohydrát)
ATEM 0,5 mg / 2 ml, roztok pro rozprašování
Proč se používá Atem? K čemu to je?
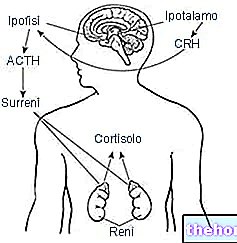
ATEM je léčivý přípravek, který obsahuje monohydrát ipratropiumbromidu, léčivou látku patřící do skupiny anticholinergních léků, která uvolňuje svaly v malých stěnách dýchacích cest v plicích.
ATEM se používá k léčbě astmatu a chronické obstrukční plicní nemoci, onemocnění způsobeného zánětem plic a dýchacích cest spojeným s astmatem.
Kontraindikace Kdy by neměl být Atem používán
Neužívejte přípravek ATEM, pokud:
- jste alergický (přecitlivělý) na „monohydrát ipratropiumbromidu nebo na kteroukoli další složku tohoto přípravku
- jste alergičtí na atropin nebo na léky patřící do stejné třídy;
- mít zvětšený objem prostaty (hypertrofie prostaty);
- máte oční onemocnění, které způsobuje zvýšený nitrooční tlak se zhoršením vidění (glaukom);
- máte problémy s močením (zadržování moči);
- má „střevní obstrukci, která se projevuje neschopností evakuace, bolestí a otoky v břiše“;
- jste těhotná nebo kojíte.
Opatření pro použití Co potřebujete vědět před užitím přípravku Atem
Pokud máte problémy se srdcem, včetně onemocnění srdečních cév (onemocnění koronárních tepen), poraďte se před užitím přípravku ATEM se svým lékařem.
Věnujte zvláštní pozornost:
- ATEM začíná působit 3-5 minut po zahájení podávání;
- pokud se lék náhodou dostane do kontaktu s vašimi očima, můžete zaznamenat poruchu oka nebo zraku, například problémy se zaostřováním obrazu (poruchy vizuální akomodace); pečlivě se poraďte se svým lékařem a nezapomeňte mu sdělit předchozí přijetí ATEM;
- pokud se vaše astma zhorší nebo se nezlepší nebo máte během léčby přípravkem ATEM větší potíže s dýcháním. Informujte svého lékaře, který může změnit vaši léčbu.
Děti
Tento lék se nedoporučuje pro děti do 3 let.
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Atem
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte nebo jste v nedávné době užíval.
Varování Je důležité vědět, že:
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, přípravek ATEM neužívejte.
Řízení dopravních prostředků a obsluha strojů
ATEM neovlivňuje schopnost řídit nebo obsluhovat stroje.
Dávkování a způsob použití Jak používat Atem: Dávkování
Vždy užívejte tento přípravek přesně podle pokynů svého lékaře. Pokud si nejste jisti, poraďte se se svým lékařem nebo lékárníkem.
Dospělí a mladiství starší 14 let
1 jednodávkový obal, 1 nebo 2krát denně, pokud lékař neurčí jinak.
Maximální dávka je 1 jednodávkový obal, 4krát denně
Děti od 3 do 14 let
Poloviční jednodávkový obal, 1 nebo 2krát denně, pokud lékař neurčí jinak.
Chcete -li užít poloviční dávku, použijte stupnici na obalu.
Maximální dávka je polovina jednodávkového obalu, 3krát denně.
Způsob podání
Tento léčivý přípravek musí být nebulizován (vyroben na velmi malé kapky) pomocí „aerosolového zařízení“ vybaveného zařízením pro podávání ústy a / nebo nosem.
ATEM užívejte vdechováním, ústy a / nebo nosem. Předepsanou dávku lze zředit přidáním stejného množství destilované vody (poměr 1: 1) do ampule nebulizátoru.
Před použitím si pečlivě přečtěte následující pokyny, které vám řeknou, co máte dělat a na co si dát pozor.
Chcete -li použít, proveďte následující operace:
Jednodávkový obal ohněte v obou směrech.
Odpojte jednodávkový obal z proužku nejprve nahoře a potom uprostřed.
Otevřete jednodávkový obal otočením klapky ve směru šipky.
Mírným tlakem na stěny jednodávkového obalu nechte lék vytéct v předepsaném množství a vložte jej do ampule s rozprašovačem (aerosolové zařízení).
Chcete-li zkontrolovat, zda jste použili poloviční dávku, postavte jednodávkový obal na světlo a porovnejte hladinu zbývajícího léku s odstupňováním v nádobě (odpovídá polovině dávky). Pokud použijete poloviční dávku, zbývající množství by mělo být zlikvidováno.
Předávkování Co dělat, když jste užil příliš mnoho přípravku Atem
Pokud užijete více přípravku ATEM, než byste měli
Pokud omylem spolknete / užijete nadměrné dávky tohoto léku, okamžitě to sdělte svému lékaři.
Pokud zapomenete užít ATEM
Pokračujte v terapii pravidelně, aniž byste zdvojnásobili další dávku. Máte -li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Atem
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Časté nežádoucí účinky (mohou postihnout až 1 z 10 lidí)
Suchá ústa
Velmi vzácné nežádoucí účinky (mohou postihnout až 1 z 10 000 lidí)
Závratě a ospalost.
Problémy se zaostřováním obrazu (poruchy vizuálního akomodace).
Problémy s močením (zadržování moči) nebo zácpa.
Poruchy srdečního rytmu (arytmie)
Nežádoucí účinky s frekvencí neznámou (frekvenci nelze z dostupných údajů určit)
Reakce způsobené alergií (přecitlivělostí).
Poruchy oka: zvýšený tlak v oku s možným zhoršením vidění, rozmazané vidění, zornice očí s různým průměrem (anisocoria), dilatace obou zornic (mydriáza).
Sípání, kašel, dušnost a sípání (paradoxní bronchospasmus)
Otok (angioedém) obličeje, očí, rtů, hrdla s obtížemi s dýcháním.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48100 41 Praha 10 Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek lék.
Expirace a retence
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Uchovávejte při teplotě do 30 ° C.
V případě použití poloviční dávky musí být množství zbývající v nádobě vyhozeno.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na krabičce za EXP. Doba použitelnosti se vztahuje k poslednímu dni daného měsíce.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Co ATEM obsahuje
Léčivou látkou je: monohydrát ipratropiumbromidu.
Jednodávkový 2ml kontejner obsahuje: 0,5218 mg monohydrátu ipratropiumbromidu, což odpovídá 0,50 mg ipratropiumbromidu.
Dalšími složkami jsou: monohydrát hydrogenfosforečnanu sodného, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, čištěná voda.
Popis vzhledu ATEM a obsahu balení
Tento léčivý přípravek je dostupný v krabičkách po 10 nebo 20 jednodávkových obalech, z nichž každý obsahuje 2 ml roztoku. Každý jednodávkový obal má dělení na poloviční dávku.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
ATEM 0,5 MG / 2 ML ROZTOK PRO NEBULIZÉR
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jednodávkový kontejner o objemu 2 ml obsahuje:
Účinná látka: monohydrát ipratropiumbromidu 0,5218 mg odpovídá ipratropiumbromidu 0,50 mg.
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Řešení nebulizátoru.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Léčba bronchiálního astmatu, chronické obstrukční plicní nemoci s astmatickou složkou.
04.2 Dávkování a způsob podání
Dospělí: jeden jednodávkový kontejner na jedno sezení v průměru 1–2krát denně. V závislosti na závažnosti může být dávka zvýšena podle lékařského předpisu až na maximálně jeden jednodávkový obal 4krát denně.
Děti (3-14 let): polovina obsahu jednodávkového obalu na jedno sezení v průměru 1–2krát denně. S ohledem na věk a závažnost může být dávka zvýšena podle lékařského předpisu až na maximálně polovinu jednodávkového obalu 3krát denně.
V případě potřeby lze roztok naředit sterilním fyziologickým roztokem v poměru 1: 1.
Jednodávkový obal má odstupňování odpovídající polovině dávky.
Chcete-li použít jednodávkový obal, proveďte následující operace:
1) ohněte jednotlivou dávku v obou směrech;
2) vyjměte jednodávkový obal z proužku nejprve nahoře a potom uprostřed;
3) otočením klapky otevřete jednodávkový obal;
4) mírným tlakem na stěny jednodávkového obalu uvolnit léčivo v předepsaném množství;
5) Umístěte jednodávkový obal proti světlu, abyste zkontrolovali přesnost poloviny dávky. Pokud použijete poloviční dávku, zbytkové množství znovu nepoužívejte.
04.3 Kontraindikace
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1; přecitlivělost na látky podobné atropinu.
Subjekty s glaukomem, hypertrofií prostaty, syndromy retence moči nebo střevní obstrukcí.
Obecně kontraindikováno v těhotenství a při kojení (viz bod 4.6).
04.4 Zvláštní upozornění a vhodná opatření pro použití
Lék by měl být podáván opatrně u koronárních a srdečních pacientů.
Pokud se látka nedbale vstříkne do očí, mohou se objevit, i když jen zřídka, poruchy zraku, byť mírné a vratné.
Aby bylo použití roztoku nebulizováno, je nutné přísně dodržovat lékařský předpis.
Předepsaná dávka se nesmí měnit a pokud nedojde k prospěchu, bude nutné ohlásit ošetřujícímu lékaři, který dávku upraví optimálním způsobem; je třeba mít na paměti, že lék začíná působit 3-5 minut po podání.
Stejně jako u jiných inhalačních podání se může vzácně objevit paradoxní bronchospasmus. V takovém případě okamžitě přerušte podávání a zahájte vhodnou terapii.
Tento lék není kontraindikován pro osoby s celiakií.
Uchovávejte tento přípravek mimo dosah dětí.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Neznámý.
04.6 Těhotenství a kojení
Při potvrzeném nebo předpokládaném těhotenství a během laktace musí být lék používán s opatrností a pod neustálým dohledem lékaře.
Fertilita viz bod 5.3.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Atem neovlivňuje schopnost řídit nebo obsluhovat stroje.
04.8 Nežádoucí účinky
Mnoho z uvedených vedlejších účinků lze přičíst anticholinergním vlastnostem společnosti Atem. V kontrolovaných klinických studiích byl nejčastěji pozorovaným vedlejším účinkem sucho v ústech.
Frekvence je definována pomocí následující konvence: Velmi časté (≥ 1/10); časté (≥ 1/100,
Frekvence nežádoucích účinků po uvedení přípravku na trh je uvedena jako neznámá.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky, ke kterým dochází po registraci léčivého přípravku, je důležité, protože umožňuje průběžné sledování poměru přínosů a rizik léčivého přípravku. Zdravotničtí pracovníci jsou požádáni, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení. "Adresa" www .agenziafarmaco.gov.it/it/responsabili “.
04.9 Předávkování
Předávkování používané v literatuře pro aerosoly pro experimentální účely nikdy nevyvolalo nepříjemné účinky.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: jiná léčiva pro obstrukční syndromy dýchacích cest pro aerosoly, anticholinergika.
ATC kód: R03BB01.
Atem obsahuje jako účinnou látku ipratropiumbromid, anticholinergní derivát k léčbě dušnosti, při chronické bronchitidě a astmatu.
Ipratropiumbromid působí lokálně na dýchací cesty v extrémně malých dávkách se zvláště vysokou specificitou účinku a značnou snášenlivostí. Ipratropiumbromid s kompetitivním mechanismem blokuje bronchiální muskarinové receptory, čímž brání působení acetylcholinu, a proto má na bronchiální úrovni anticholinergní účinek. Bronchospasmolytický účinek začíná 3–5 minut po vdechnutí a přetrvává 4–6 hodin. Podávání ipratropiumbromidu lze realizovat také v případě akutního bronchospasmu střední intenzity: v tomto případě se zlepšení stavu průdušek začne projevovat do 10 minut po vdechnutí.
05.2 Farmakokinetické vlastnosti
Kinetické studie s ipratropiumbromidem značeným C14 ukázaly, že po inhalaci jednorázové dávky 555 mcg je maximální koncentrace v krvi dosažená mezi 1. a 3. hodinou zanedbatelná a rovná se 0,033% celkové inhalované dávky a vztahuje se na objem plazmy.
05.3 Předklinické údaje vztahující se k bezpečnosti
Akutní toxicita
LD50 (samec myši, per os): 1001 mg / kg;
LD50 (samice myši, per os): 1083 mg / kg;
LD50 (krysa samec, per os): 1663 mg / kg;
LD50 (samice krysy, per os): 1779 mg / kg;
LD50 (pes, per os): 1300 mg / kg;
LD50 (krysa, opice pro aerosol): chybí.
Subakutní a chronická toxicita
Krysy: per os (55 týdnů), dávka až 200 mg / kg; inhalace (26 týdnů), dávka až 512 mcg / den.
Psi: per os (52 týdnů), dávka až 75 mg / kg.
Opice: inhalace (6 měsíců), dávka až 1600 mcg / den.
Králíci: per os (4 týdny), dávka až 400 mg / den.
Použití ipratropiumbromidu k inhalaci, a to ani při maximálních dávkách, nevykazovalo žádný toxický účinek a žádný rozdíl mezi ošetřenými a kontrolními zvířaty.
Testy teratogeneze a plodnosti
Byly použity myši, krysy a králíci. U žádného ze tří druhů nebyl zjištěn nárůst malformací ani v žádném případě změn, které by mohly souviset s léčbou ipratropiumbromidem.
Potomci nevykazovali organické změny. V prenatálním a postnatálním vývojovém procesu nebyly pozorovány žádné léze. Ipratropiumbromid nepoškodil genetickou kapacitu mužů a žen.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Monobazický monohydrát fosforečnanu sodného, dihydrát hydrogenfosforečnanu sodného, chlorid sodný, čištěná voda.
06.2 Neslučitelnost
Irelevantní.
06.3 Doba platnosti
2 roky.
Toto období je určeno pro specialitu řádně skladovanou as neporušeným obalem.
06.4 Zvláštní opatření pro skladování
Uchovávejte při teplotě do 30 ° C.
06.5 Charakter vnitřního obalu a obsah balení
Vnitřní obal: jednodávkové polypropylenové nádoby s odstupňováním poloviční dávky, znovu uzavíratelné. Vnější obal: potištěná lepenková krabice.
Krabice s 10 nebo 20 jednodávkovými obaly po 2 ml
06.6 Návod k použití a zacházení
Nepoužitý léčivý přípravek a odpad z tohoto přípravku musí být zlikvidován v souladu s místními předpisy.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
PROMEDICA s.r.l., Via Palermo 26 / A - Parma
Prodejce na prodej: CHIESI FARMACEUTICI S.p.A., Via Palermo 26 / A - Parma
08.0 REGISTRAČNÍ ČÍSLO
024153052 0,5 mg / 2 ml roztok pro rozprašování - 10 jednodávkových obalů
024153064 0,5 mg / 2 ml roztok pro rozprašování - 20 jednodávkových obalů
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
06/06/2000
10.0 DATUM REVIZE TEXTU
Stanovení AIFA z července 2015.