Účinné látky: ranitidin (ranitidin hydrochlorid)
Ranidil 75 mg potahované tablety
Příbalové letáky Ranidil jsou k dispozici pro velikosti balení:- RANIDIL 150 mg potahované tablety, RANIDIL 300 mg potahované tablety
- RANIDIL 150 mg šumivé tablety, RANIDIL 300 mg šumivé tablety
- RANIDIL 150 mg / 10 ml sirup
- RANIDIL 50 mg / 5 ml injekční roztok pro intravenózní podání
- Ranidil 75 mg potahované tablety
Proč se používá Ranidil? K čemu to je?
Léčivou látkou Ranidilu 75 mg je ranitidini hydrochloridum, což odpovídá 75 mg ranitidinu.
Ranidil 75 mg tablety patří do skupiny léků známých jako antagonisté histaminových H2 receptorů. Antagonisté H2 receptorů dočasně snižují produkci kyseliny v žaludku, aby odstranili příčinu pálení žáhy a zažívacích potíží z překyselení. Dostatečné množství kyseliny v žaludku na podporu trávení.
Tablety Ranidil 75 mg můžete užívat, pokud trpíte onemocněními způsobenými žaludeční kyselinou, jako je pálení žáhy a zažívací potíže způsobené překyselením.
Kontraindikace Kdy by Ranidil neměl být používán
Neužívejte Ranidil 75 mg
- jestliže jste alergický / á (přecitlivělý / á) na ranitidin nebo na kteroukoli další složku přípravku Ranidil 75 mg (viz bod: Další informace).
Opatření pro použití Co potřebujete vědět před užitím Ranidilu
Zvláštní opatrnosti při užívání přípravku Ranidil 75 MG je zapotřebí
- máte závažné problémy s ledvinami nebo játry.
- musíte pravidelně podstupovat lékařské prohlídky.
- jste ve středním věku nebo starší a poprvé máte žaludeční nevolnost, nebo pokud se vaše potíže zhoršují.
- užívat léky s lékařským předpisem nebo bez něj.
- máte podrážděný žaludek a neúmyslně hubnete.
- užívejte nesteroidní protizánětlivé léky, jako jsou léky proti bolesti (NSAID: např. aspirin nebo ibuprofen), zvláště pokud jste v minulosti trpěli žaludečním vředem.
- někdy prodělali epizodu akutní porfyrie (vrozené onemocnění, které způsobuje změnu ve výrobě hemového pigmentu pro produkci krve).
- je starší
- mít problémy s dýcháním
- má oslabený imunitní systém
- je diabetik
Poraďte se se svým lékařem, pokud se vás cokoli z výše uvedeného týká nebo se to v minulosti vyskytlo.
Interakce Které léky nebo potraviny mohou ovlivnit účinek Ranidilu
Ranidil může ovlivnit účinnost některých léků, které užíváte. Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte nebo jste v nedávné době užíval (a) :
- k prevenci srážení krve (např. warfarin)
- k léčbě infekcí (např. ketokonazolu, atazanaviru nebo delaviridinu)
- ke kontrole hladiny cukru v krvi (např. glipizid)
- k léčbě úzkosti a poruch spánku (např. triazolam, midazolam)
- k léčbě určitých typů rakoviny (např. gefitnib)
- k léčbě nepravidelného srdečního tepu (např. prokainamid a acetylprokainamid)
- k léčbě zánětu žaludku, dvanáctníku nebo jícnu (např. sukralfát)
Užívání Ranidilu 75 mg s jídlem a pitím
Ranidil 75 mg můžete užít kdykoli, s jídlem nebo pitím nebo bez něj.
Varování Je důležité vědět, že:
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se se svým lékařem nebo lékárníkem dříve, než začnete tento přípravek užívat.
Ranitidin prochází placentou a je vylučován do mateřského mléka. Z tohoto důvodu byste neměli užívat Ranidil 75 mg tablety během těhotenství nebo během kojení bez předchozí konzultace s lékařem.
Řízení dopravních prostředků a obsluha strojů
Nejsou k dispozici dostatečné údaje o účincích na schopnost řídit a obsluhovat stroje.
Dávka, způsob a doba podání Jak používat Ranidil: Dávkování
Vždy užívejte Ranidil 75 mg přesně podle pokynů svého lékaře. Pokud máte pochybnosti, poraďte se se svým lékařem nebo lékárníkem. Obvyklá dávka je uvedena níže.
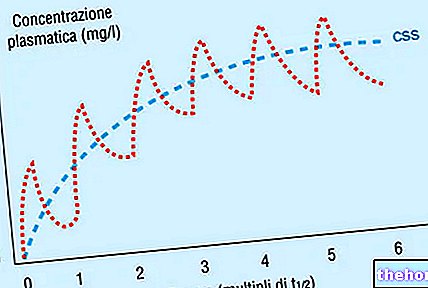
Jakmile máte pálení žáhy nebo zažívací potíže způsobené překyselením, v kteroukoli denní nebo noční dobu si můžete vzít tabletu. Ranidil 75 mg vytváří dlouhodobý účinek, který začíná přibližně 30 minut po užití tablety. Účinek dosahuje svého vrcholu po dvou hodinách a může trvat až dvanáct hodin. To je důvod, proč většina pacientů nepotřebuje více než jednu nebo dvě tablety každých 24 hodin.
V případě potřeby však můžete během 24 hodin užít až čtyři tablety.
Nepřekračujte doporučené dávky.
Tabletu Ranidil 75 mg můžete spolknout s tekutinou.
Děti do 16 let
Použití Ranidilu 75 mg není indikováno u dětí mladších 16 let.
Snížená funkce ledvin
Pokud máte problémy s ledvinami, měli byste se před použitím poradit se svým lékařem, protože může být nutné upravit dávkování.
Předávkování Co dělat, když jste užil příliš mnoho Ranidilu
Jestliže jste užil (a) více Ranidilu 75 mg, než jste měl (a), měli byste okamžitě kontaktovat svého lékaře nebo lékárníka.
Máte -li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka
Nežádoucí účinky Jaké jsou vedlejší účinky Ranidilu
Podobně jako všechny léky, může mít i Ranidil 75 mg nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Pro klasifikaci frekvence nežádoucích účinků byla použita následující konvence: velmi časté (> 1/10), časté (> 1/100, 1/1 000, 1/10 000,
Méně časté nežádoucí účinky (1 ze 100 až 1 z 1000 pacientů):
- bolest břicha
- zácpa
- nevolnost.
Tyto příznaky se téměř vždy během léčby zlepšují.
Vzácné nežádoucí účinky (1 z 1 000 až 1 z 10 000 pacientů):
- alergické reakce (vyrážka s intenzivním svěděním a kopřivkou), náhlé nahromadění tekutiny v kůži a sliznicích (například v krku nebo jazyku), potíže s dýcháním a / nebo svědění a vyrážka, často jako alergická reakce (angioneurotický edém) , horečka, tlak na hrudi v důsledku stažení svalů v dýchacích cestách (bronchospasmus), nízký krevní tlak (hypotenze) a bolest na hrudi *.
- vyrážka.
- Obecně se během léčby normalizuje mírné zvýšení plazmatického kreatinu.
Velmi vzácné nežádoucí účinky (méně než 1 z 10 000 pacientů):
- některé krevní poruchy, jako je leukopenie (nedostatek bílých krvinek doprovázený zvýšeným rizikem infekce), trombocytopenie (nedostatek krevních destiček doprovázený tvorbou modřin a sklonem ke krvácení). Pancytopenie (celkový nedostatek krvinek) nebo agranulocytóza (velmi závažné snížení počtu bílých krvinek, které je doprovázeno náhlou a vysokou horečkou, závažným zánětem hrdla a vředy v ústech), někdy s hypoplazií dřeně (a stav, kdy se kostní dřeň nevytvořila správně) nebo aplázie dřeně (porucha, při které dřeň neprodukuje dostatek nových buněk).
- anafylaktický šok (prudký pokles krevního tlaku, bledost, úzkost, slabý a rychlý puls, lepkavá kůže, snížené vědomí) způsobený náhlým a značným rozšířením cév v důsledku silné přecitlivělosti na specifické látky. *
- deprese, halucinace a reverzibilní mentální zmatek. Tyto nežádoucí účinky byly hlášeny hlavně u těžce nemocných pacientů, starších osob a pacientů s ledvinami.
- bolest hlavy (někdy silná), závratě a reverzibilní a nedobrovolné pohybové poruchy.
- reverzibilní rozmazané vidění.
- pomalá srdeční frekvence (bradykardie).
- některé poruchy ve vodivém systému srdce (atrioventrikulární blok), které vedou k poruchám srdečního rytmu (tachykardie).
- zánět cév (vaskulitida).
- akutní zánět slinivky břišní (akutní pankreatitida).
- průjem
- zánět jater (hepatitida), obvykle reverzibilní, který může být spojen se žloutenkou (zežloutnutí kůže nebo očí). svědění.
- kožní vyrážka s červenými a hrbolatými (vlhkými) skvrnami (multiformní erytém).
- vypadávání vlasů (alopecie).
- bolest svalů nebo kloubů (artralgie a myalgie).
- zánět ledvin, doprovázený krví v moči, horečka a bolest v boku (akutní intersticiální nefritida).
- reverzibilní impotence.
- abnormální vývoj mléčné žlázy u mužů (gynekomastie) a spontánní ztráta mléka z prsu nesouvisející s porodem nebo kojením (galaktorea).
Nežádoucí účinky s frekvencí neznámou (frekvenci nelze z dostupných údajů určit):
dušnost*.
* tyto nežádoucí účinky jsou hlášeny po jedné dávce.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48100 41 Praha 10 Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
Expirace a retence
Ranidil 75 mg uchovávejte v původním obalu při teplotě nepřesahující 30 ° C.
Uchovávejte mimo dohled a dosah dětí.
Nepoužívejte Ranidil 75 mg po uplynutí doby použitelnosti, uvedené na obalu za „EXP“. Doba použitelnosti se vztahuje k poslednímu dni v měsíci.
OBSAH BALENÍ A DALŠÍ INFORMACE
Co Ranidil 75 mg obsahuje
- Léčivou látkou je ranitidin (ve formě ranitidin hydrochloridu).
- Dalšími složkami jsou mikrokrystalická celulóza, magnesium -stearát, hypromelosa, oxid titaničitý (E171), triacetin, syntetický červený oxid železitý (E172).
Jak Ranidil 75 mg vypadá a obsah balení
Ranidil 75 mg potahované tablety jsou růžové a pětiúhelníkového tvaru. Na jedné straně tabletu je uvedeno „75“.
Tablety jsou k dispozici v blistrech.
Jedno balení Ranidilu 75 mg obsahuje 5 nebo 10 tablet.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Chcete-li mít přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
TABLETY RANIDIL 75 MG potažené filmem
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna potahovaná tableta Ranidil 75 mg obsahuje 75 mg ranitidinu (jako hydrochlorid).
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Potahované tablety.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Symptomatická léčba zažívacích potíží způsobených překyselením a pálením žáhy.
04.2 Dávkování a způsob podání
Dospělí:
Užijte jednu tabletu Ranidil 75 mg, když pocítíte příznaky, ve dne i v noci.
Léčba 1 nebo 2 tabletami denně je u většiny pacientů dostačující. Za 24 hodin lze užít až 4 tablety.
Tablety není nutné užívat s jídlem.
Pacienti by měli být poučeni, aby se poradili se svým lékařem nebo lékárníkem, pokud příznaky přetrvávají, zhoršují se nebo pokračují po 14 dnech.
Pacienti s poškozením ledvin:
U pacientů s poruchou funkce ledvin může dojít k akumulaci ranitidinu vedoucí ke zvýšeným plazmatickým koncentracím (hladiny odbaveníkreatininu pod 50 ml / min). (Viz bod 4.4)
Děti:
Použití tablet Ranidil 75 mg u dětí mladších 16 let se nedoporučuje.
04.3 Kontraindikace
Ranitidinové přípravky jsou kontraindikovány u pacientů se známou přecitlivělostí na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Rakovina žaludku
Před zahájením léčby ranitidinem u pacientů se žaludečním vředem nebo u pacientů středního nebo staršího věku s nově vzniklými nebo nově upravenými dyspeptickými příznaky nebo neúmyslným úbytkem hmotnosti doprovázenými dyspeptickými příznaky by měl být pacient vyloučen. Možná maligní povaha, protože léčba ranitidin může maskovat příznaky rakoviny žaludku, a proto může oddálit diagnostiku.
Nemoc ledvin
Ranitidin je eliminován ledvinami, proto jsou plazmatické hladiny léčiva zvýšeny u pacientů s poruchou funkce ledvin (clearance kreatininu nižší než 50 ml / min). Dávka by měla být upravena, jak je uvedeno v bodě 4.2. „Pacienti s poškozením ledvin“. U takových pacientů není použití přípravků Ranitidin vhodné bez lékařského dohledu.
Podle vzácných klinických zpráv může ranitidin upřednostňovat výskyt akutních záchvatů porfyrie. Ranitidin by proto neměl být podáván pacientům s anamnézou akutní porfyrie.
U pacientů, jako jsou starší lidé, lidé s chronickým plicním onemocněním, diabetici nebo imunokompromitovaní, může existovat zvýšené riziko rozvoje komunitní pneumonie. Velká epidemiologická studie prokázala zvýšené riziko rozvoje komunitní pneumonie u pacientů, kteří stále užívali samotný ranitidin, ve srovnání s těmi, kteří léčbu ukončili, s pozorovaným upraveným zvýšením relativního rizika o 1,82% (95% CI 1,26 - 2,64).
U pacientů užívajících nesteroidní protizánětlivá léčiva souběžně s léčbou ranitidinem se doporučuje pravidelné lékařské sledování, zvláště pokud jsou starší nebo mají v anamnéze peptický vřed.
Pacientům s poruchou funkce ledvin / jater, těm, kteří jsou pod nepřetržitým lékařským dohledem, a těm, kteří užívají jakékoli jiné léky (předepsané i předepsané na předpis) je třeba doporučit, aby se před použitím poradili se svým lékařem.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Ranitidin může ovlivnit absorpci, metabolismus nebo renální vylučování jiných léků. Změna farmakokinetických parametrů může vyžadovat úpravu dávky ovlivněného léčiva nebo přerušení léčby.
Interakce probíhají prostřednictvím různých mechanismů, včetně:
1) Inhibice systému oxygenázy se smíšenou funkcí navázaného na jaterní cytochrom P450:
ranitidin v obvyklých terapeutických dávkách nezesiluje účinek léčiv, která jsou inaktivována tímto enzymatickým systémem, jako je diazepam, lidokain, fenytoin, propranolol a teofylin.
Byly hlášeny změny protrombinového času s kumarinovými antikoagulancii (např. Warfarinem). Vzhledem k úzkému terapeutickému indexu se při současné léčbě ranitidinem doporučuje pečlivé sledování zvýšení a snížení protrombinového času.
2) Soutěž o renální tubulární sekreci:
ranitidin, částečně eliminovaný kationtovým systémem, může ovlivnit odbavení jiných drog eliminovaných tímto způsobem. Vysoké dávky ranitidinu (např. Dávky používané při léčbě Zollinger-Ellisonova syndromu) mohou snížit vylučování prokainamidu a N-acetylprokainamidu, což má za následek zvýšení plazmatických hladin těchto léčiv.
3) Změna pH v žaludku:
může být ovlivněna biologická dostupnost některých léků. To může mít za následek jak zvýšenou absorpci (např. Triazolam, midazolam, glipizid), tak sníženou absorpci (např. Ketokonazol, atazanavir, delaviridin, gefitnib).
Neexistuje žádný důkaz interakce mezi ranitidinem a amoxicilinem a metronidazolem.
Absorpci ranitidinu lze snížit, pokud jsou současně podávány vysoké dávky (2 g) sukralfátu, hydroxidu hořečnatého nebo hlinitého.
K tomuto účinku nedochází, pokud jsou tyto látky podávány po intervalu 2 hodin.
04.6 Těhotenství a kojení
Plodnost
Nejsou k dispozici žádné údaje o účinku ranitidinu na lidskou plodnost. Studie na zvířatech neprokázaly žádné účinky na mužskou a ženskou plodnost (viz bod 5.3).
Těhotenství
Ranitidin překračuje placentární bariéru. Stejně jako ostatní léky by měl být podáván během těhotenství, pouze pokud je to považováno za nezbytně nutné.
Čas krmení
Ranitidin se vylučuje do mateřského mléka. Stejně jako ostatní léky by měl být podáván během laktace, pouze pokud je to považováno za nezbytně nutné.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Nejsou k dispozici dostatečné údaje o účincích na schopnost řídit a obsluhovat stroje.
04.8 Nežádoucí účinky
Pro klasifikaci nežádoucích účinků byla použita následující konvence: velmi časté (≥1 / 10), časté (≥1 / 100,
Četnosti nežádoucích účinků byly odhadnuty na základě údajů o spontánním hlášení po uvedení přípravku na trh.
Poruchy krve a lymfatického systému
Velmi vzácné: změny počtu krvinek (leukopenie, trombocytopenie). Ty jsou obvykle reverzibilní. Agranulocytóza nebo pancytopenie, někdy doprovázená hypoplazií nebo aplazií kostní dřeně.
Poruchy imunitního systému
Vzácné: reakce přecitlivělosti (kopřivka, angioneurotický edém, horečka, bronchospasmus, hypotenze a bolest na hrudi).
Velmi vzácné: anafylaktický šok.
Není známo: dušnost
Tyto příhody byly hlášeny po podání jedné dávky.
Psychiatrické poruchy
Velmi vzácné: reverzibilní mentální zmatenost, deprese, halucinace.
Výše uvedené příhody byly hlášeny hlavně u těžce nemocných pacientů, starších pacientů a pacientů s ledvinami.
Poruchy nervového systému
Velmi vzácné: bolest hlavy (někdy silná), závratě a reverzibilní mimovolní pohyby.
Oční poruchy
Velmi vzácné: reverzibilní rozmazané vidění.
Byly hlášeny některé případy rozmazaného vidění způsobené změnou akomodace.
Srdeční patologie
Velmi vzácné: jako u ostatních antagonistů H2 receptorů bradykardie, atrioventrikulární blok a tachykardie.
Cévní patologie
Velmi vzácné: vaskulitida.
Gastrointestinální poruchy
Velmi vzácné: akutní pankreatitida průjem.
Méně časté: bolest břicha, zácpa, nevolnost (tyto příznaky se téměř vždy během léčby zlepšují).
Poruchy jater a žlučových cest
Vzácné: přechodné a reverzibilní změny jaterních testů.
Velmi vzácné: obvykle reverzibilní hepatitida (hepatocelulární, hepatocanalicular nebo smíšená) se žloutenkou nebo bez ní.
Poruchy kůže a podkožní tkáně
Vzácné: kožní vyrážka, svědění.
Velmi vzácné: multiformní erytém, alopecie.
Poruchy svalové a kosterní soustavy a pojivové tkáně
Velmi vzácné: příznaky postihující muskuloskeletální systém, jako je artralgie a myalgie.
Poruchy ledvin a močových cest
Vzácné: zvýšení plazmatického kreatininu (obvykle mírné; během léčby se normalizuje).
Velmi vzácné: akutní intersticiální nefritida.
Nemoci reprodukčního systému a prsu
Velmi vzácné: reverzibilní impotence, změny libida. Příznaky prsu, patologie a změny (jako je gynekomastie a galaktorea).
Pediatrická populace:
Bezpečnost ranitidinu byla dobře hodnocena u dětí ve věku 0 až 16 let s chorobami souvisejícími s kyselinami a byla dobře snášena s profilem nežádoucích účinků podobným jako u dospělých.
K dispozici jsou omezené údaje o dlouhodobé bezpečnosti, zejména pokud jde o růst a vývoj.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky, které se vyskytnou po registraci léčivého přípravku, je důležité, protože umožňuje průběžné sledování poměru prospěchu a rizika léčivého přípravku.Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48100 41 Praha 10 Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek
04.9 Předávkování
Příznaky a příznaky
Klinické zkušenosti s předávkováním jsou omezené. Akutní požití až do 18 g orálně hlášené bylo spojeno s přechodnými nežádoucími účinky podobnými těm, které se vyskytují v běžné klinické zkušenosti. U pacientů bylo také hlášeno zvracení, podrážděnost a nespavost. Děti a ospalost a nevolnost u dospělých .
Léčba
V případě předávkování by měla být podle potřeby použita symptomatická a podpůrná léčba.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antagonisté H2 receptorů.
ATC kód: A02B A02.
Ranitidin je specifický antagonista rychle působících histaminových H2 receptorů. Inhibuje bazální a stimulovanou sekreci žaludeční kyseliny, snižuje jak objem, tak obsah kyseliny a pepsinu v sekretu. Ranitidin má dlouhé trvání účinku a jedna dávka 75 mg účinně potlačuje sekreci žaludeční kyseliny až na 12 hodin. Klinické studie ukázaly, že Ranidil 75 mg může zmírnit příznaky až na dvanáct hodin.
05.2 Farmakokinetické vlastnosti
Biologická dostupnost ranitidinu se trvale pohybuje kolem 50%. Po orálním podání dávky 75 mg jsou vrcholové plazmatické koncentrace, normálně v rozmezí 236-270 ng / ml, dosaženy po 2-3 hodinách. Plazmatické koncentrace ranitidinu jsou úměrné dávce až do 300 mg včetně.
Ranitidin není rozsáhle metabolizován. Eliminace léčiva probíhá hlavně tubulární sekrecí. Poločas eliminace je 2-3 hodiny.
Ve studiích eliminace hmotnostní bilance prováděných se 150 mg ranitidinu značeného tritiem bylo 93% intravenózní dávky vyloučeno močí a 5% stolicí; 60-70% perorální dávky bylo vyloučeno močí a 26% stolicí. Analýza provedená na moči vyloučené během prvních 24 hodin po podání ukázala, že 70% intravenózní dávky a 35% perorální dávky je eliminováno beze změny. Metabolismus ranitidinu je po perorálním i intravenózním podání podobný; přibližně 6% dávky se vylučuje močí jako N-oxid, 2% jako S-oxid, 2% jako demethylranitidin a 1-2% jako analog kyseliny furoové.
05.3 Předklinické údaje vztahující se k bezpečnosti
Konkrétně žádné údaje.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Mikrokrystalická celulóza
Stearát hořečnatý
Hypromelóza
Oxid titaničitý E171
Triacetin
Syntetický červený oxid železitý E172
06.2 Neslučitelnost
Žádný.
06.3 Doba platnosti
3 roky.
06.4 Zvláštní opatření pro skladování
Uchovávejte při teplotě do 30 ° C.
06.5 Charakter vnitřního obalu a obsah balení
Tablety v blistrech z hliníku / PVC / polyamidu v balení po 5, 6, 10, 12, 24 nebo 48 tabletách.
Na trhu nemusí být všechny velikosti balení.
06.6 Návod k použití a zacházení
Žádný.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
A. Menarini Industrie Farmaceutiche Riunite S.r.l. - Via Sette Santi, 3 - Florencie
Licencováno společností GlaxoSmithKline S.p.A.
08.0 REGISTRAČNÍ ČÍSLO
Balení 5 tablet: A.I.C. n. 024447157
Balení 10 tablet: A.I.C. n. 024447169
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
19. prosince 1996/31. Prosince 2009
10.0 DATUM REVIZE TEXTU
Prosinec 2014















----tiamfenicolo.jpg)