Účinné látky: klotrimazol
1% krém Canesten
Proč se Canesten používá? K čemu to je?
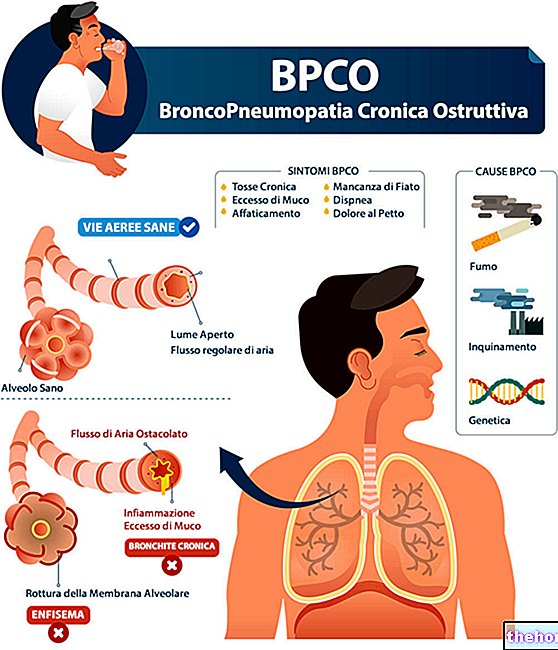
Canesten obsahuje klotrimazol, který je antifungální (antimykotický) pro dermatologické použití, tj. Působí lokálně eliminací kožních plísní.
Canesten se používá k léčbě mykóz (plísní) kůže a kožních záhybů, jako je pityriasis versicolor, kožní kandidóza, tinea pedis nebo atletická noha, tinea corporis.
Kontraindikace Kdy by Canesten neměl být používán
Nepoužívejte přípravek Canesten
- jestliže jste alergický (á) na klotrimazol nebo na kteroukoli další složku tohoto přípravku (uvedenou v bodě 6).
Opatření pro použití Co potřebujete vědět před užitím přípravku Canesten
Poraďte se svým lékařem nebo lékárníkem před použitím přípravku Canesten, pokud jste v minulosti trpěl těmito problémy (relaps mykózy).
Použití nedýchatelných plenek se nedoporučuje po aplikaci léku na plenkové vyrážky.
Vyhnout se očnímu kontaktu. Nepožívejte.
Použití, zejména pokud se prodlužuje, přípravků pro topické použití (aplikovaných na kůži), může způsobit senzibilizační jevy, jako je erytém (zarudnutí lokalizované v oblasti kůže, kde je lék aplikován) a svědění. v takovém případě přerušte léčbu a poraďte se se svým lékařem nebo lékárníkem.
Interakce Které léky nebo potraviny mohou změnit účinek přípravku Canesten
Další léčivé přípravky a přípravek Canesten
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte, které jste v nedávné době užíval (a) nebo které možná budete užívat.
Nejsou známy žádné léky, které by mohly změnit účinek přípravku Canesten.
Canesten s jídlem
Nejsou známy žádné potraviny, které by mohly upravit účinek přípravku Canesten.
Varování Je důležité vědět, že:
Těhotenství a kojení
Pokud jste těhotná nebo kojíte, domníváte se, že můžete být těhotná, nebo plánujete otěhotnět, poraďte se před použitím tohoto přípravku se svým lékařem nebo lékárníkem.
Těhotenství
Údaje o použití klotrimazolu v těhotenství jsou omezené.V rámci preventivních opatření se vyvarujte používání přípravku Canesten v prvním trimestru těhotenství.
Čas krmení
Během léčby přípravkem Canesten ukončete kojení, protože lék může přecházet do mateřského mléka.
Řízení dopravních prostředků a obsluha strojů
Tento léčivý přípravek nemá žádný nebo má zanedbatelný vliv na schopnost řídit nebo obsluhovat stroje.
Canesten obsahuje cetostearylalkohol
Může způsobit lokální kožní reakce (např. Kontaktní dermatitidu).
Dávka, způsob a doba podání Jak používat Canesten: Dávkování
Vždy používejte tento přípravek přesně podle pokynů v této příbalové informaci nebo podle pokynů svého lékaře nebo lékárníka. Pokud máte pochybnosti, poraďte se se svým lékařem nebo lékárníkem.
Krém je zvláště vhodný pro ošetření bezsrstých (bezsrstých) oblastí pokožky.
Krém Canesten by měl být aplikován v malých množstvích 2-3krát denně, v souladu s ošetřovanými částmi.
Vzhledem k vysoké fungicidní aktivitě přípravku Canesten obvykle stačí k ošetření povrchu o velikosti dlaně použití malého množství krému.
Canesten krém by měl být aplikován lehkým třením po pečlivě omytém a vysušeném ošetřovaném dílu.
Varování: nepřekračujte uvedené dávky bez lékařského doporučení.
Trvání léčby
Obecně k vymizení projevů stačí doba léčby tři až čtyři týdny.
Pokračujte v léčbě krémem Canesten alespoň 2 týdny po vymizení symptomů, abyste konsolidovali získané terapeutické výsledky a vyhnuli se reinfekcím.
V případě, že po 3-4 týdnech nepřetržitého používání nezaznamenáte znatelné výsledky, poraďte se se svým lékařem. Poraďte se se svým lékařem, pokud se porucha vyskytuje opakovaně nebo pokud jste si všimli nedávných změn v jejích charakteristikách.
Poznámky ke zdravotní výchově
Aby se předešlo mykóze a jejím relapsům, je užitečné dodržovat některá hygienická pravidla, jako například:
- Vyhněte se chůzi naboso na veřejných místech, jako jsou bazény, tělocvičny, hotelové pokoje atd.
- Pokud sportujete, používejte prodyšnou a pohodlnou obuv, jejíž vložky je třeba pravidelně měnit nebo prát.
- Omezte používání oděvů obsahujících syntetická vlákna.
- Plenky dítěte často vyměňujte, aby se zabránilo hromadění moči nebo výkalů na kůži.
- Před přivítáním do domácího prostředí podrobte psy a kočky veterinárnímu vyšetření.
- Pokud se u člena rodiny objeví mykóza, dodržujte další hygienická opatření, například oddělené oblečení a praní na vysoké teplotě.
Předávkování Co dělat, když jste užil příliš mnoho přípravku Canesten
Jestliže jste použil (a) více přípravku Canesten, než jste měl (a)
Neočekává se žádné riziko akutní intoxikace, protože je nepravděpodobné, že by k němu došlo po jednorázové kožní aplikaci předávkování (prodloužená aplikace za podmínek vedoucích k absorpci) nebo neúmyslném perorálním podání. Neexistuje žádné specifické antidotum.
V případě náhodného požití / požití krému Canesten okamžitě informujte svého lékaře nebo jděte do nejbližší nemocnice.
Jestliže jste zapomněl (a) použít přípravek Canesten
Pokračujte v léčbě dávkou předepsanou lékařem.
Máte -li jakékoli další otázky týkající se používání tohoto přípravku, zeptejte se svého lékaře nebo lékárníka.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Canesten
Podobně jako všechny léky, může mít i tento přípravek nežádoucí účinky, které se ale nemusí vyskytnout u každého.
U přípravku Canesten byly hlášeny následující nežádoucí účinky, jejichž četnost není známa:
Poruchy imunitního systému: alergická reakce (projevuje se mdlobami, poklesem krevního tlaku, dušností, kopřivkou).
Poruchy kůže a podkožní tkáně: puchýře, nepříjemné pocity nebo bolest, otoky, erytém (zarudnutí kůže), podráždění, olupování (ztráta buněk z vnější vrstvy kůže), svědění, vyrážka, pálení.
Dodržování pokynů obsažených v příbalové informaci snižuje riziko nežádoucích účinků.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo prostřednictvím národního systému hlášení nežádoucích účinků na adrese „https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse“. Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
Expirace a retence
Uchovávejte tento přípravek mimo dohled a dosah dětí.
Nepoužívejte tento přípravek po uplynutí doby použitelnosti uvedené na obalu. Datum exspirace se vztahuje k poslednímu dni uvedeného měsíce. Datum exspirace se vztahuje na neotevřený produkt a správně skladovaný.
Nepoužívejte 1% krém Canesten po 3 měsících od prvního otevření.
Nevyhazujte žádné léčivé přípravky do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Je důležité mít vždy k dispozici informace o léku, proto si uschovejte krabičku i příbalovou informaci.
Složení a léková forma
Co Canesten obsahuje
- Aktivní složkou je klotrimazol. 100 g krému obsahuje 1 g klotrimazologu.
- Dalšími složkami jsou: sorbitan monostearát, polysorbát 60, cetylpalmitát, cetostearylalkohol, oktyldodekanol, benzylalkohol, čištěná voda.
Jak Canesten vypadá a obsah balení
Canesten je dodáván ve formě krému pro použití na kůži.
Obsah balení je 30 g.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
CANESTEN UNIDIE 1% KRÉM
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1% smetany
100 g smetany obsahuje:
aktivní princip:
bifonazol 1 g.
Pomocné látky se známými účinky: cetylstearylalkohol, sorbitan monostearát, polysorbát 60.
Úplný seznam pomocných látek viz 6.1.
03.0 LÉKOVÁ FORMA
Krém.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Léčba dermatomykóz způsobených dermatofyty, sacharomycety, jinými patogenními houbami: mykóza nohy a ruky, mykóza trupu (tinea corporis), mykóza kožních záhybů (tinea inguinalis), onychomykóza, pityriasis versicolor, povrchová kandidóza.
04.2 Dávkování a způsob podání
Pro úplné uzdravení je nezbytné kontrolované a dostatečně dlouhé používání přípravku Canesten Unidie.
Je však vhodné nepřerušovat terapii bezprostředně po vymizení akutních zánětlivých projevů a subjektivních symptomů, ale dodržovat následující průměrné doby léčby v závislosti na typu infekce, rozsahu a lokalizaci samotné infekce:
Způsob podání
Pokud není předepsáno jinak, Canesten Unidie by měl být aplikován v malých množstvích na infikované části lehkou masáží jednou denně, nejlépe večer před spaním.
Malé množství krému je obecně dostatečné k ošetření povrchu zhruba rovného dlani.
Pediatrická populace
U dětí nebyla bezpečnost a účinnost přípravku Canesten Unidie prokázána; dokud není získáno dostatečné množství údajů, není používání produktu u těchto osob uvedeno.
04.3 Kontraindikace
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Použití, zejména prodloužené, přípravků pro topické použití může způsobit senzibilizační jevy, které se projevují zarudnutím a svěděním; v tomto případě je nutné léčbu přerušit a zahájit vhodnou terapii.
Totéž bude provedeno v případě vývoje rezistentních mikroorganismů.
Pacienti se známými reakcemi z přecitlivělosti na jiná imidazolová antimykotika (např. Ekonazol, klotrimazol, mikonazol) by měli léčivé přípravky obsahující bifonazol používat s opatrností.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Dostupné údaje naznačují možnou interakci mezi topickým bifonazolem a warfarinem se zvýšeným protrombinovým časem.
Pokud se Canesten Unidie používá u pacientů léčených warfarinem, měli by být vhodně sledováni.
04.6 Těhotenství a kojení
Těhotenství
Předklinické údaje o bezpečnosti a farmakokinetické údaje u člověka neposkytují žádné údaje o účincích na matku a dítě při užívání bifonazolu během těhotenství (viz bod 5.3).
Nejlepší je vyhnout se užívání bifonazolu během prvního trimestru těhotenství.
Čas krmení
Vylučování do mléka bylo studováno na zvířatech. Dostupné farmakodynamické / toxikologické údaje na zvířatech ukázaly, že bifonazol a jeho metabolity přecházejí do mateřského mléka (viz bod 5.3).
Není známo, zda se bifonazol vylučuje do lidského mléka.
Kojení by mělo být během léčby bifonazolem přerušeno.
Plodnost
Předklinické studie neprokázaly poškození mužské ani ženské plodnosti (viz bod 5.3).
04.7 Účinky na schopnost řídit a obsluhovat stroje
Canesten Unidie nemá žádný nebo má zanedbatelný vliv na schopnost řídit a obsluhovat stroje
04.8 Nežádoucí účinky
Následující nežádoucí účinky jsou odvozeny ze spontánních hlášení po uvedení přípravku na trh a není možné definovat jejich četnost.
Celkové poruchy a reakce v místě aplikace
Bolest v místě podání, periferní edém (v místě podání).
Poruchy kůže a podkožní tkáně
Kontaktní dermatitida, alergická dermatitida, erytém, svědění, vyrážka, kopřivka, puchýře, odlupování kůže, ekzém, suchá kůže, podráždění kůže, macerace kůže, pocit pálení.
Tyto vedlejší účinky jsou reverzibilní po přerušení léčby.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky vyskytující se po registraci léčivého přípravku je důležité, protože umožňuje průběžné sledování poměru přínosů a rizik léčivého přípravku. Žádáme zdravotnické pracovníky, aby hlásili podezření na nežádoucí účinky prostřednictvím národního systému hlášení. "Adresa https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Předávkování
• Nebyly hlášeny žádné případy předávkování.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: deriváty imidazolu a triazolu.
ATC kód: DO1AC10.
Bifonazol inhibuje biosyntézu ergosterolu na dvou různých úrovních, čímž se odlišuje od ostatních azolových derivátů a dalších antimykotik, které působí pouze na jedné úrovni. Inhibice syntézy ergosterolu vede ke strukturálnímu a funkčnímu poškození cytoplazmatické membrány houby.
Canesten Unidie působí proti infekcím způsobeným dermatofyty, sacharomycesy (kvasinky), plísněmi a dalšími patogenními houbami, jako je Malassezia furfur.
Hodnota MIC pro uvedené druhy hub je v rozmezí pod 0,062-4 (-16) mcg / ml substrátu.Bifonazol vykazuje výraznou fungicidní aktivitu proti dermatofytům, zejména Tricophyton spp. Úplného fungicidního účinku je již dosaženo při koncentraci asi 5 mcg / ml a po expozici 6 h. Na kvasinky, např. Candida, v koncentraci 1-4 mcg / ml je působení bifonazolu primárně fungistatické, zatímco v koncentrace 20 mcg / ml je fungicidní.
Varianty primární rezistence vnímavých druhů hub jsou velmi vzácné.
Výzkum neposkytuje důkazy o vývoji sekundární rezistence u primárně vnímavých druhů.
05.2 Farmakokinetické vlastnosti
Bifonazol dobře proniká do infikovaných vrstev kůže.
6 hodin po podání dosahují koncentrace v různých vrstvách kůže od 1 000 mcg / cm3 ve vnějších vrstvách epidermis (stratum corneum) do 5 mcg / cm3 v papilární vrstvě. Všechny stanovené koncentrace jsou tedy v rozmezí antifungální aktivitu in vitro.
Doba pobytu v kůži, měřená ochranným působením proti infekci u morčat, je 48-72 hodin.
Farmakokinetické studie po topické aplikaci na neporušenou lidskou kůži ukázaly, že je absorbováno pouze malé množství bifonazolu (0,6-0,8% dávky); výsledné sérové koncentrace byly vždy pod mezí detekce (tj.
Bifonazol u potkanů prochází placentární bariérou.
05.3 Předklinické údaje vztahující se k bezpečnosti
Předklinické údaje jsou založeny na konvenčních studiích toxicity a genotoxicity po jednorázové dávce.
Účinky indukce jaterních enzymů byly pozorovány u dávek nad 50 mg / kg po dobu až 13 týdnů); opakované dávky rovné nebo vyšší než 3 mg / kg určily jasné známky utrpení na úrovni různých orgánů a zejména jaterní tukové degenerace.
Úrovně expozice jsou však vyšší než maximální expozice, která má význam pro klinické použití.
Bifonazol neprokázal mutagenní účinky v následujících testech: „Salmonella / mikrosom“, „Mikronukleový test“ a „dominantní smrtící“ test.
Byly provedeny studie na králících za účelem hodnocení dermální snášenlivosti. Po subakutní topické aplikaci bifonazolového krému (což odpovídá 3 mg / kg bifonazolu) po dobu 3 týdnů byl pozorován mírný dráždivý účinek (otok). V primárním testu dráždivosti byla snášenlivost sliznice a očí dobrá.
Studie kancerogenity nebyly s bifonazolem provedeny.
Při perorálních dávkách vyšších než 40 mg / kg nebylo pozorováno žádné poškození mužské a ženské plodnosti (u potkanů).
V reprodukčních toxikologických studiích na králících poskytla perorální dávka 30 mg / kg tělesné hmotnosti a vyšší dávky embryonální a fetotoxické výsledky včetně letality. U potkanů není bifonazol v perorálních dávkách až 100 mg / kg embryotoxický, ale zpomaluje vývoj kostry plodu, což je pravděpodobně vedlejším účinkem mateřské toxicity (snížení hmotnosti).
Vzhledem k nízké absorpci účinné látky kůží mají tyto výsledky malý význam pro klinické použití.
Studie na potkanech ukázaly, že bifonazol prochází placentární bariérou a je vylučován do mléka.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
1% smetany:
monostearát sorbitanu;
polysorbát 60;
spermaceti;
cetylstearylalkohol;
oktyldodekanol;
benzylalkohol;
čištěná voda.
06.2 Neslučitelnost
Irelevantní.
06.3 Doba platnosti
5 let.
Jelikož jde o přípravek s více dávkami, může opakované otevření obalu vystavit léčivo mikrobiální kontaminaci, proliferaci a / nebo chemicko-fyzikální degradaci; proto by lék již neměl být používán po 16 měsících od prvního otevření.
06.4 Zvláštní opatření pro skladování
Skladujte při teplotě nepřesahující 25 ° C
06.5 Charakter vnitřního obalu a obsah balení
Hliníková trubka vnitřně chráněna epoxidovými pryskyřicemi.
Krém: tuba 30 g.
06.6 Návod k použití a zacházení
Vyhnout se očnímu kontaktu.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Bayer S.p.A. - Viale Certosa 130 - Milán
08.0 REGISTRAČNÍ ČÍSLO
Canesten Unidie AIC 026045029
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
20.08.1985 31/5/2010
10.0 DATUM REVIZE TEXTU
Stanovení AIFA ze dne: února 2015