Pro toxikodynamiku, pro lepší nebo horší, jsou pojmy chápané pro farmakodynamiku převzaty. Pojmy interakce s receptorem nespecifickým a specifickým způsobem, interakce substrátu (toxické) -receptoru, afinita toxického k receptoru, účinnost a nakonec antagonismus musí být dobře známy. Tyto koncepty nejsou převzaty, protože se jedná o stejné koncepty, které byly pro drogu znázorněny; nicméně se budeme podrobně věnovat některým typickým mechanismům působení toxických látek.
Toxický, stejně jako lék, působí s cílovou molekulou, což bude první bod studie.
JAKÝ JE CÍL TOXIKOLOGIE? Cílem toxické látky je buňka, která se skládá z proteinů, lipidů, nukleových kyselin a dalších složek.
Druhým bodem studie je typ vazby mezi toxickou a cílovou buňkou, což je důležitý faktor závažného účinku toxické látky. Jak víme, spojení může být reverzibilní a nevratné.
Pokud je toxická látka reverzibilně vázána, může se oddělit a účinek je méně závažný, než když se váže na cíl kovalentní vazbou, proto je nevratný.

Třetí bod studie spočívá v důsledcích interakce mezi toxickou a cílovou buňkou.
Co modifikuje toxicitu vazbou na cílovou molekulu?
Může dojít k modifikaci produkce energie, takže buňka neprodukuje ATP a jde proti smrti; může dojít k modifikaci homeostázy intracelulárního vápníku, což je jeden z nejdůležitějších druhých poslů, nebo nakonec může dojít ke změně plazmatické membrány.
Toto jsou všechny příklady buněčných funkcí, které jsou toxické změněny po navázání na cílové místo.
CÍLOVÉ MOLEKULY
Jak již bylo zmíněno dříve, buňka se skládá z proteinů, lipidů, nukleových kyselin a dalších složek.
Možné cílové molekuly jsou tedy:
- PROTEINY (membrána, enzymy ...);
- LIPIDS (membránové fosfolipidy);
- SKUPINY -SH (proteiny cytoskeletu);
- NUCLEIC ACIDS (bude vysvětleno v článku o karcinogenezi a poškození DNA).
1) CÍLY PROTEINŮ
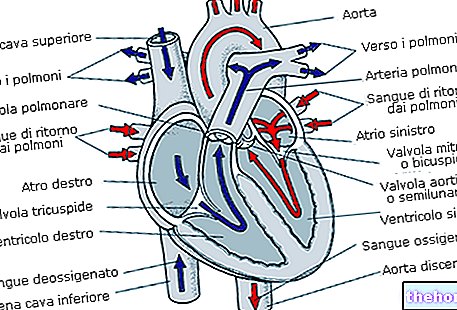
Zde je několik příkladů proteinových cílů. V prvním příkladu uvažujeme o „hemoproteinu, kterým je hemoglobin“, a o velmi podobné toxické látce, kterou je oxid uhelnatý (CO). Oxid uhelnatý, který je 250krát mnohem podobnější než kyslík, se váže na skupinu -EME hemoglobinu, čímž brání transportu kyslíku.Tkanivové buňky umírají na ANEMICKOU HYPOXII, protože nedostávají potřebný kyslík pro buněčné dýchání.
V druhém příkladu je vzata v úvahu molekula enzymatického proteinu, což je Cyt C oxidáza a související toxický kyanid. Cyt C oxidáza je enzym, který patří do řetězce přenosu elektronů. Buněčné dýchání probíhá na úrovni mitochondrií a Cyt C oxidáza využívá kyslík, aby zajistila, že jsou z mitochondrií vypuzeny čtyři ionty H +; toto vypuzení vodíkových iontů tvoří potenciální rozdíl nezbytný pro syntézu ATP. Enzym je blokován kyanidem , Cyt C oxidáza již nepoužívá molekulární kyslík, optimální gradient protonů se netvoří mimo mitochondrie; v důsledku toho buňka nesyntetizuje ATP. Také v tomto případě jsou buňky proti smrti v důsledku hypoxie; mluvíme zejména o CYTOTOXIC HYPOXIA.
Mezi všemi proteinovými cíli najdeme receptory, které byly vysvětleny v obecné farmakologii. Nejdůležitější toxiny, jako je nikotin a strychnin, mohou interagovat s různými receptory.
2) LIPIDOVÉ CÍLY
Lipidy nejvíce ovlivněné volnými radikály jsou membrány. Volný radikál z chemického hlediska vzniká proto, že mezi dvěma atomy nedochází k „heterolýze“, proto se netvoří dva ionty s homogenním nábojem, ale dochází k „homolýze“.
Homolýza je charakterizována nerovnoměrným rozložením nábojů.

Volné radikály se tvoří z vnějších látek (xenobiotika), ale také uvnitř našeho organismu (volné radikály kyslíku). Můžeme tedy říci, že volné radikály se mohou tvořit jak zvenčí, tak zevnitř našeho organismu.
Jak tyto radikály vznikají?
Volné kyslíkové radikály mohou vznikat při změně parciálního napětí kyslíku v buňce, takže dochází k náhlým změnám tlaku kyslíku. Tento náhlý nedostatek kyslíku podporuje vznik radikálních druhů v ischemických (mozkových) nebo srdečních tkáních. Radikálními druhy kyslíku jsou především SUPEROXIDOVÝ ANION a OXIDRIL. Nedostatek antioxidantů (vitamíny A, C a E), stárnutí buněk, xenobiotika a nakonec akutní a / nebo chronické zánětlivé stavy jsou všechny jevy, které mohou vést k tvorba volných radikálů.

Buňka může reagovat na tato možná poškození v důsledku nástupu volných kyslíkových radikálů, protože má zvláštní enzymy, které působí proti aktivitě radikálů.

Další články na téma "Toxikodynamika"
- Paracetamol a jaterní nekróza
- Toxicita a toxikologie
- Zaměřte molekuly toxických látek