Účinné látky: bacampicilin
Bacacil 1200mg potahované tablety
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Chcete-li mít přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
TABLETY BACACIL 1200 MG potažené FILMEM
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna potahovaná tableta obsahuje:
Aktivní princip:
Bacampicillini hydrochloridum 1200 mg
Pomocné látky:
Laktóza
Úplný seznam pomocných látek viz bod 6.1
03.0 LÉKOVÁ FORMA
potahované tablety
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Bacacil se ukázal být účinný při léčbě různých infekcí způsobených citlivými kmeny grampozitivních a gramnegativních bakterií, zejména:
- infekce horních a dolních cest dýchacích, udržované citlivými kmeny pneumokoků, streptokoků, stafylokoků neprodukujících penicilinázu a H. influenzae;
- infekce genitourinárního systému, udržované citlivými kmeny E-colienterokoky, stafylokoky nevytvářející penicilinázu, P. mirabilis A N. gonorrhoeae;
- infekce kůže a měkkých tkání, udržované citlivými kmeny stafylokoků produkujících ne-penicilinázu, streptokoky a enterokoky;
- střevní infekce z citlivých kmenů Shigella a Salmonella (včetně S. typhosa);
- odontostomatologické infekce akutní a chronické udržované citlivými zárodky.
04.2 Dávkování a způsob podání
Dospělí a děti starší 7 let: 2 400 mg rozdělených do dvou denních dávek.
04.3 Kontraindikace
Bacacil je kontraindikován u subjektů se známou přecitlivělostí na léčivou látku, na penicilin a / nebo cefalosporiny nebo na kteroukoli pomocnou látku uvedenou v bodě 6.1. Současné podávání disulfiramu je navíc kontraindikováno.
Subjekty s infekční mononukleózou (viz také bod 4.4).
04.4 Zvláštní upozornění a vhodná opatření pro použití
U subjektů léčených penicilinem byly hlášeny závažné a někdy fatální reakce z přecitlivělosti (anafylaktoidní typ). Ačkoli je anafylaxe běžnější po parenterální terapii, je také známa u subjektů užívajících perorální peniciliny.Tyto reakce se snadněji vyskytují u subjektů s anamnézou přecitlivělosti na penicilin a / nebo reakcí z přecitlivělosti na více alergenů.
Byly hlášeny subjekty s „přecitlivělostí na penicilin v anamnéze, u nichž se při léčbě cefalosporiny vyskytly závažné reakce. Před zahájením léčby penicilinem důkladné vyšetření předchozích reakcí z přecitlivělosti na peniciliny, cefalosporiny a další alergeny.
Dojde -li k alergické reakci, je třeba lék vysadit a zahájit příslušnou terapii. Závažné anafylaktoidní reakce vyžadují okamžitou naléhavou léčbu epinefrinem. Podle potřeby by měl být také podáván kyslík, intravenózní steroidy a asistovaná ventilace včetně intubačních procesů.
Jako u všech přípravků obsahujících antibiotika je pro výskyt necitlivých zárodků včetně plísní nezbytné neustálé pozorování. Pokud dojde k superinfekci, lék by měl být vysazen a / nebo by měla být zahájena vhodná terapie.
Kolitida spojená s antibiotiky byla hlášena téměř u všech antibakteriálních látek a její závažnost může být mírná až život ohrožující (viz bod 4.8). Proto je důležité zvážit tuto diagnózu u pacientů, kteří mají průjem během nebo po podání jakéhokoli antibiotika. Pokud dojde k kolitidě související s antibiotiky, je třeba okamžitě vysadit bacampicilin, poradit se s lékařem a zahájit vhodnou léčbu. V této situaci jsou peristaltické léky kontraindikovány.
Během dlouhodobé léčby by měla být prováděna periodická hodnocení jaterního, renálního a hematopoetického systému.
Vysoké procento pacientů s mononukleózou léčených ampicilinem má vyrážku.Z tohoto důvodu by pacientům s mononukleózou nemělo být podáváno žádné antibiotikum z rodiny ampicilinů. Není známo, zda je zvýšený výskyt vyrážky ampicilinu způsoben samotným alopurinolem nebo často přítomnou hyperurikémií u těchto pacientů. Stále nejsou k dispozici žádné údaje o výskytu vyrážky u pacientů léčených bacampicilinem a alopurinolem. Pokud hledáte možnou glykosurii pomocí klinitestu nebo Benediktova nebo Fehlingova činidla, je třeba mít na paměti, že vysoké koncentrace ampicilinu v moči mohou vést k falešně pozitivním výsledkům. Z tohoto důvodu se doporučuje použití enzymatických činidel na bázi glukózooxidázy.
Během používání ampicilinu u těhotných žen byl pozorován reverzibilní pokles hladin celkového konjugovaného estriolu, glukuronát estriolu, konjugovaného estronu a estradiolu v krvi.
Tablety obsahují laktózu, proto by pacienti se vzácnými dědičnými problémy s intolerancí galaktózy, nedostatkem laktázy nebo malabsorpcí glukózy a galaktózy neměli tento lék užívat.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Souběžné užívání alopurinolu a ampicilinu může zvýšit procento exantematózních kožních reakcí Souběžné podávání probenecidu a bacampicilinu může mít za následek zvýšení a prodloužení hladin bacampicilinu v krvi v průběhu času.
Bakteriostatická antibiotika, jako je erythromycin, chloramfenikol a tetracykliny, mohou interferovat s baktericidním účinkem bacampicilinu.
Synergický terapeutický účinek je znám mezi polosyntetickými peniciliny a amino glykosidy.
Některé peniciliny mohou snižovat účinnost perorálních kontraceptiv, proto by měly být pacientky dostatečně informovány.
04.6 Těhotenství a kojení
U těhotných žen by měl být lék podáván v případě skutečné potřeby pod přímým dohledem lékaře. U těhotných žen byl během používání ampicilinu pozorován reverzibilní pokles hladin konjugovaného celkového estriolu, estriol -glukuronátu, konjugovaného estronu a estradiolu v krvi.
Antibiotická třída ampicilinů se vylučuje do mateřského mléka, a proto by podávání BACACILu (bacampicillinu) mělo být pečlivě hodnoceno u kojících matek.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Nebyl hlášen žádný vliv bacampicilinu na schopnost řídit a obsluhovat stroje.
04.8 Nežádoucí účinky
Stejně jako u jiných penicilinů mohou nastat sekundární reakce, které jsou v podstatě omezeny na jevy citlivosti. Tyto reakce se snadněji vyskytují u subjektů s pozitivní anamnézou alergie, astmatu, senné rýmy, kopřivky. Byly hlášeny následující sekundární reakce související s použitím orálně aktivních širokospektrálních penicilinů:
Gastrointestinální poruchy : glositida, stomatitida, epigastrická bolest, nevolnost, zvracení, průjem, zánět žaludku, enterokolitida, černý a patinózní jazyk. V kontrolovaných klinických studiích byl výskyt průjmu u přípravku Bacacil (bacampicilin) přibližně o jednu desetinu vyšší než u perorálního ampicilinu. Stejně jako u všech širokospektrálních antibiotik je i během léčby možné detekovat kolitidu. Pseudomembranózní během léčby.
Poruchy imunitního systému : stejně jako u ampicilinu byly s určitou frekvencí hlášeny následující: makulopapulární vyrážka a erytém; byla také hlášena kopřivka, multiformní erytém a příležitostně exfoliativní dermatitida. Kopřivku, další kožní vyrážky a projevy podobné sérové nemoci lze kontrolovat antihistaminiky a v případě potřeby systémovými kortikosteroidy. Pokud se takové reakce vyskytnou, je třeba léčbu přípravkem Bacacil (Bacampicillin) přerušit, pokud to podle názoru lékaře neohrožuje léčený stav. život pacienta a lze jej léčit pouze terapií bacampicilinem.
Použití přípravku BACACIL (bacampicilin), stejně jako u všech penicilinů k perorálnímu podání, může vést k závažným a někdy fatálním reakcím z přecitlivělosti (anafylaktické) (viz bod 4.4 Zvláštní upozornění a opatření pro použití).
Poruchy jater a žlučových cest : Mírné zvýšení SGOT bylo zaznamenáno zejména u kojenců. Význam těchto údajů není znám.
Poruchy krve a lymfatického systému : jsou hlášeny stavy anémie, trombocytopenie, trombocytopenická purpura, eozinofilie, leukopenie a agranulocytóza. Po přerušení léčby jsou obvykle reverzibilní a jsou považovány za jevy přecitlivělosti.
Poruchy ledvin a močových cest: v literatuře byly hlášeny případy akutní intersticiální nefritidy vyskytující se během léčby penicilinem, ale Bacacilu neexistují žádné podobné zprávy.
Hlášení podezření na nežádoucí účinky
Hlášení podezření na nežádoucí účinky, ke kterým dochází po registraci léčivého přípravku, je důležité, protože umožňuje průběžné sledování poměru přínosů a rizik léčivého přípravku. Zdravotničtí pracovníci jsou požádáni, aby hlásili jakékoli podezření na nežádoucí účinky prostřednictvím národního systému hlášení. "Adresa www. agenziafarmaco.gov.it/it/responsabili.
04.9 Předávkování
V literatuře dosud nebyly zaznamenány žádné případy předávkování.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Beta-laktamová antibakteriální léčiva, peniciliny.
ATC kód: J01CA06.
Jakmile je bacampicilin podroben hydrolýze ampicilinu, vykazuje antibakteriální aktivitu, zjevně se stejným antibakteriálním spektrem jako ampicilin. Ten má široké spektrum a je účinný proti mnoha grampozitivním a gramnegativním bakteriím. Mechanismus účinku ampicilinu, stejně jako u ostatních penicilinů, se projevuje inhibicí syntézy mukopeptidů, základních složek bakteriální stěny .
Antibiotická třída ampicilinů je deaktivována enzymem beta-laktamázou syntetizovaným některými kmeny Enterobacter, Citrobacter, Haemophilus inflenzae a Escherichia coli a z mnoha kmenů Stafylokok a ze Protestuje indol-pozitivní. Třída antibiotik ampicilinů nebyla shledána aktivní Pseudomonas, Klebsiella A Serratia spp.
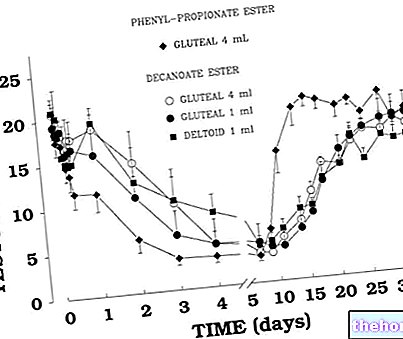
05.2 Farmakokinetické vlastnosti
Bacampicilin se rychle a téměř úplně vstřebává v žaludku a dvanáctníku. U lidí jsou vrcholy v sérových koncentracích asi 2–3krát vyšší než píky získané po ekvimolárních dávkách ampicilinu.
Vazba na sérové proteiny je nízká, řádově 18%. Přibližně 80% orálně podané dávky bacampicilinu se nachází v moči v aktivní formě. Porucha funkce ledvin má za následek snížení rychlosti vylučování ampicilinu.Krevní frekvence se snižují hemodialýzou.
05.3 Předklinické údaje vztahující se k bezpečnosti
Toxikologické studie na různých druzích zvířat ukázaly, že bacampicilin v dávkách podobných dávkám používaným v terapii je dobře snášen. Nemá vliv na reprodukční aktivitu a nemá teratogenní ani mutagenní účinek.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Laktóza, mikrokrystalická celulóza, stearát hořečnatý, hypromelóza, oxid titaničitý, mastek, makrogol 6000.
06.2 Neslučitelnost
Irelevantní.
06.3 Doba platnosti
3 roky.
06.4 Zvláštní opatření pro skladování
Skladujte při teplotě nepřesahující 25 ° C
06.5 Charakter vnitřního obalu a obsah balení
Polyvinylchloridové blistry
Krabička s 12 tabletami po 1200 mg
06.6 Návod k použití a zacházení
Žádné zvláštní pokyny.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Meda Pharma S.p.A. - Via Felice Casati 20 - 20124 Milán - Itálie
08.0 REGISTRAČNÍ ČÍSLO
BACACIL 1200: AIC č. 024130054
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
31. května 2000/1. Června 2010
10.0 DATUM REVIZE TEXTU
Duben 2017