Co je Stayveer - Bosentan a k čemu se používá?
Stayveer je léčivý přípravek, který obsahuje účinnou látku bosentan. Je indikován k léčbě pacientů s plicní arteriální hypertenzí (PAH) třídy III ke zlepšení cvičební kapacity a symptomů. PAH je patologický stav, při kterém je zvýšen tlak v plicních tepnách. „Třída“ označuje závažnost onemocnění: „třída III“ zahrnuje silné omezení fyzické aktivity. PAH může být:
- primární (bez identifikované nebo rodinné příčiny);
- způsobené sklerodermií (nebo progresivní systémovou sklerózou, onemocněním charakterizovaným abnormálním růstem pojivové tkáně podporující kůži a další orgány);
- způsobené vrozenými srdečními vadami (přítomnými od narození) se zkraty (malformace dýchacích cest), které způsobují abnormální průtok krve mezi srdcem a plícemi.
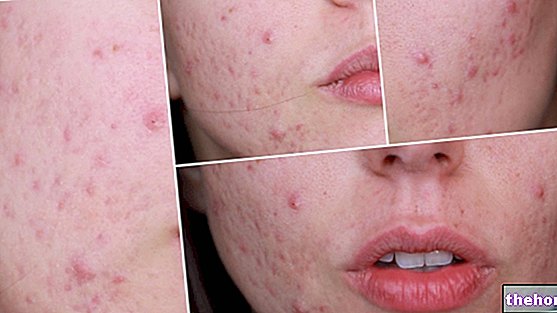
- Zlepšení bylo také pozorováno u pacientů s PAH třídy II. „Třída II“ zahrnuje mírné omezení fyzické aktivity. Stayveer lze použít také u dospělých s progresivní systémovou sklerózou, u níž špatný krevní oběh způsobený touto nemocí způsobil výskyt „digitálních vředů“ (zánět prstů rukou) a nohou) Cílem společnosti Stayveer je snížit počet nových digitálních vředů.
Tento léčivý přípravek je stejný jako přípravek Tracleer, který je již registrován v Evropské unii (EU). Společnost, která přípravek Tracleer vyrábí, souhlasila, že jeho vědecká data mohou být použita pro Stayveer („informovaný souhlas“).
Jak se Stayveer - Bosentan používá?
Výdej přípravku Stayveer je vázán na lékařský předpis a léčbu by měl zahájit a sledovat lékař, který má zkušenosti s léčbou PAH nebo progresivní systémové sklerózy. Stayveer je k dispozici ve formě tablet (62,5 mg a 125 mg), které je třeba spolknout a zapít vodou. Tablety se užívají ráno a večer. U dospělých je počáteční dávka 62,5 mg dvakrát denně po dobu čtyř týdnů, poté se zvyšuje na obvyklou dávku 125 mg dvakrát denně. U dětí s PAH je použitá dávka založena na tělesné hmotnosti a obvykle začíná dávkou 2 mg na kilogram dvakrát denně. Další informace naleznete v příbalové informaci. Lékař by měl posoudit odpověď pacienta na Stayveer a stanovit potřebu další léčby po osmi týdnech u pacientů s PAH, u kterých nebylo hlášeno zlepšení, a také pravidelně u pacientů s progresivní systémovou sklerózou s pokračujícími digitálními vředy. Pokud se lékař rozhodne léčbu přípravkem Stayveer přerušit, dávku je třeba snižovat postupně. Pacientům léčeným přípravkem Stayveer musí být poskytnuto speciální memorandum, které shrnuje hlavní informace o bezpečnosti tohoto léčivého přípravku.
Jak Stayveer - Bosentan funguje?
Účinná látka přípravku Stayveer, bosentan, inhibuje přirozeně se vyskytující hormon zvaný endotelin-1 (ET-1), který způsobuje zúžení krevních cév. Stayveer proto způsobuje „expanzi krevních cév. PAH je oslabující onemocnění, při kterém dochází k závažnému zúžení plicních cév. Způsobuje velmi vysoký tlak v cévách, které přenášejí krev z pravé strany srdce do plic. K tomuto tlaku dochází. Snižuje množství kyslíku, které krev může přenášet do plic, což ztěžuje fyzickou aktivitu. Rozšířením těchto cév dochází ke snížení krevního tlaku a zlepšení symptomů. U pacientů s progresivní systémovou sklerózou a probíhajícími digitálními vředy zlepšuje bosentan krevní oběh v prstech na rukou a nohou a brání vzniku nových digitálních vředů.
Jaký přínos přípravku Stayveer - Bosentan prokázal v průběhu studií?
V případě PAH byl přípravek Stayveer zkoumán ve čtyřech hlavních studiích: dvě studie zahrnující celkem 245 dospělých s PAH třídy III nebo IV, primární nebo způsobené sklerodermií, jedna studie zahrnující 54 dospělých s PAH třídy III související s vrozenými srdečními vadami jako studie 185 pacientů s PAH třídy II. Studie porovnávaly Stayveer s placebem (látkou, která nemá na tělo žádný účinek), obě byly přidány ke standardní terapii.Hlavním měřítkem účinnosti bylo, jak daleko mohou pacienti dojít za šest minut (způsob měření cvičební kapacity) ; studie onemocnění třídy II se však také zabývala změnou odolnosti vůči průtoku krve v plicních cévách (indikátor zúžení cév). U PAH třídy III nebo IV, primárního nebo způsobeného sklerodermií, tyto dvě studie odhalily, že pacienti léčení přípravkem Stayveer byli schopni překonat větší vzdálenosti než pacienti léčení placebem po 16 týdnech léčby (o 44 metrů více ve studii větší velikosti); počet pacientů s PAH třídy IV byl však příliš malý na to, aby podporoval užívání léčiva v této skupině. Podobné výsledky se objevily také u pacientů s vrozenými srdečními vadami. U subjektů s PAH třídy II Stayveer vyvolal 23% snížení krve cévní rezistence ve srovnání s placebem po šesti měsících léčby, ale vzdálenost, kterou by pacienti mohli ujít za šest minut, byla v těchto dvou skupinách podobná. Byla také provedena studie na 19 dětech ve věku 3 až 15 let, ve kterých došlo ke zlepšení srdce a byly pozorovány arteriální parametry. V případě progresivní systémové sklerózy s digitálními vředy byly dvě studie porovnávány s přípravkem Stayveer s placebem u celkem 312 dospělých. Míra účinnosti byla založena na počtu nových digitálních vředů, které se vyvinuly v průběhu studie. Jedna ze studií také zkoumala účinky Stayveeru na uzdravení 190 pacientů měřením času, který je zapotřebí na úplné vyhojení daného digitálního vředu u každého pacienta. Společnost Stayveer byla při snižování tvorby nových digitálních vředů účinnější než placebo. V první studii uváděli pacienti užívající přípravek Stayveer v průměru 1,4 nového digitálního vředu po 16 týdnech ve srovnání s 2,7 vředy u pacientů užívajících placebo. Podobné výsledky byly pozorovány ve druhé studii po 24 týdnech léčby, avšak Stayveer neměl žádný vliv na digitální hojení vředu.
Jaká rizika jsou spojena s přípravkem Stayveer - Bosentan?
U PAH jsou nejčastějšími vedlejšími účinky přípravku Stayveer (které mohou postihnout více než 1 z 10 lidí) bolest hlavy a abnormální testy jaterních funkcí. U pacientů s digitálními vředy jsou nejčastějšími nežádoucími účinky přípravku Stayveer (které mohou postihnout více než 1 osobu z 10) abnormální jaterní testy, otoky a zadržování tekutin. Vzhledem k riziku rozvoje jaterních problémů vám lékař změří hladiny jaterních enzymů před léčbou a každý měsíc během léčby přípravkem Stayveer. Úplný seznam nežádoucích účinků hlášených v souvislosti s přípravkem Stayveer je uveden v příbalové informaci. • pacienti léčení cyklosporinem A (léčivý přípravek, který působí na imunitní systém). Úplný seznam omezení je uveden v příbalové informaci.
Na základě čeho byl přípravek Stayveer - Bosentan schválen?
Výbor pro humánní léčivé přípravky (CHMP) agentury rozhodl, že přínosy přípravku Stayveer převyšují jeho rizika, a doporučil, aby byl schválen k použití v EU.
Jaká opatření jsou přijímána k zajištění bezpečného a účinného používání přípravku Stayveer - Bosentan?
Byl vypracován plán řízení rizik, který má zajistit, aby byl Stayveer používán co nejbezpečněji. Na základě tohoto plánu byly do souhrnu údajů o přípravku a příbalové informace společnosti Stayveer přidány informace o bezpečnosti, včetně příslušných opatření, která by měli zdravotničtí pracovníci a pacienti dodržovat. Kromě toho společnost, která vyrábí Stayveer, poskytne informační sadu pro předepisující lékaře a informační brožuru pro pacienty v každém členském státě, aby vysvětlila bezpečnost přípravku Stayveer (se zvláštním ohledem na jeho účinky na játra a v těhotenství) a jeho interakce. Společnost se také zavazuje pečlivě sledovat distribuci léčivého přípravku v každém členském státě a shromažďovat informace o jeho použití u pacientů s progresivní systémovou sklerózou s pokračujícími vředy v prstech.
Další informace o Stayveer - Bosentan
Dne 24. června 2013 udělila Evropská komise „Registraci“ přípravku Stayveer platnou v celé Evropské unii. Další informace o terapii Stayveer naleznete v příbalové informaci (součástí zprávy EPAR) nebo se poraďte se svým lékařem nebo lékárníkem. Poslední aktualizace tohoto souhrnu: 06-2013.
Informace o Stayveer - Bosentan zveřejněné na této stránce mohou být zastaralé nebo neúplné. Správné použití těchto informací najdete na stránce Prohlášení a užitečné informace.