Účinné látky: fenobarbital
Luminale® 200 mg / ml injekční roztok pro intramuskulární podání
Luminale® 100 mg tablety
Příbalové letáky Luminale jsou k dispozici pro balení: - Luminale® 200 mg / ml injekční roztok pro intramuskulární podání, Luminale® 100 mg tablety
- Tablety Luminale® 15 mg
Indikace Proč se používá Luminale? K čemu to je?
Farmakoterapeutická skupina
Barbituráty
Terapeutické indikace
Luminale® je indikován hlavně jako obecné sedativum, se zvláštním zřetelem na epilepsii a všechny stavy vyžadující dlouhotrvající sedaci. Luminale® je zvláště užitečný při fokální epilepsii a grand mal. Může být použit jako hypnotikum a při detoxikaci chronického barbiturismu.
Kontraindikace Kdy by Luminale neměl být používán
Přecitlivělost na barbituráty, porfyrie, renální a jaterní insuficience, závažné srdeční choroby, akutní intoxikace alkoholem, analgetika, hypnotika.
Opatření pro použití Co potřebujete vědět, než začnete užívat Luminale
Fenobarbital může být návykový. Pokračující terapie indukuje tvorbu jaterních enzymů, které urychlují metabolismus některých léků, jako jsou antikoagulancia, některá antibiotika, adrenální steroidy atd.
Přípravky Hypericum perforatum by neměly být užívány současně s léčivými přípravky obsahujícími fenobarbital kvůli riziku snížení plazmatických hladin a snížené terapeutické účinnosti fenobarbitalu (viz Interakce).
Náhlé přerušení léčby u epileptických pacientů může vyvolat status epilepticus.
Pacientkám, které mohou otěhotnět nebo jsou v plodném věku, by měla být poskytnuta odborná pomoc.
Pokud pacientka plánuje otěhotnět, měla by být přehodnocena potřeba antiepileptické léčby.
U potomků matek léčených antiepileptikem se riziko vrozených vad zvyšuje dvakrát až třikrát, nejčastěji hlášeným rozštěpem rtu, kardiovaskulárními malformacemi a vadami neurální trubice.
Polyterapie antiepileptiky může být spojena s vyšším rizikem vrozených vývojových vad než monoterapie. Proto je důležité, aby byla monoterapie praktikována, kdykoli je to možné. Náhlé přerušení antiepileptické léčby by nemělo být prováděno kvůli nebezpečí obnovení záchvatů, které by mohly mít vážné důsledky pro matku i dítě.
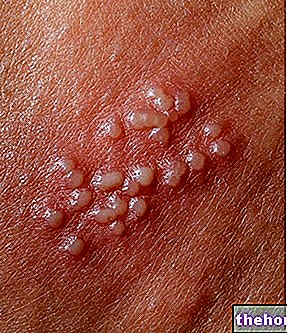
Při používání přípravku Luminale byly hlášeny život ohrožující kožní vyrážky (Stevens-Johnsonův syndrom, toxická epidermální nekrolýza), které se zpočátku objevují jako kulaté červené skvrny nebo kruhové skvrny často doprovázené puchýři ve střední části kufru.
Mezi další příznaky patří vředy v ústech, krku, nosu, genitáliích a zánět spojivek (červené a oteklé oči)
Tyto život ohrožující vyrážky jsou často doprovázeny příznaky podobnými chřipce. Vyrážka se může vyvinout do rozsáhlých puchýřů nebo odlupování kůže.
Nejvyšší riziko závažných kožních reakcí se vyskytuje v prvních 8 týdnech léčby.
Pokud se u vás při použití přípravku Luminale vyvinul Stevens-Johnsonův syndrom nebo toxická epidermální nekrolýza, přípravek Luminale se již nesmí používat.
Pokud se u vás objeví kožní vyrážka nebo tyto kožní příznaky, přestaňte Luminale užívat, naléhavě se poraďte s lékařem a informujte ho, že užíváte tento lék.
Interakce Které léky nebo potraviny mohou ovlivnit účinek Luminale
Účinnost fenobarbitalu může být snížena současným podáváním přípravků na bázi Hypericum perforatum, což je způsobeno indukcí enzymů odpovědných za metabolismus léčiv přípravky na bázi Hypericum perforatum, které by proto neměly být podávány současně s fenobarbitalem. Indukční účinek může přetrvávat nejméně 2 týdny po ukončení léčby přípravky Hypericum perforatum. Pokud pacient současně užívá přípravky Hypericum perforatum, měly by být monitorovány hladiny fenobarbitalu v krvi a léčba přípravky Hypericum perforatum ukončena. Úroveň fenobarbitalu v krvi se může zvýšit zastavením Hypericum perforatum. Může být nutné upravit dávkování fenobarbitalu.
Účinek alkoholu se zvyšuje a příjem alkoholických nápojů by měl být omezen Kombinace s jinými psychotropními léky a antihistaminiky vyžaduje zvláštní opatrnost a ostražitost lékaře, aby se předešlo neočekávaným nežádoucím účinkům interakce.
Varování Je důležité vědět, že:
Léčba fenobarbitalem snižuje pozornost a prodlužuje dobu reflexů: pacienti musí být na to upozorněni, aby se vyhnuli řízení vozidel nebo provádění operací, které kvůli své nebezpečnosti vyžadují integritu bdělosti.
U malého počtu pacientů léčených antiepileptiky, jako je Luminale, se objevily myšlenky na sebepoškozování nebo sebevraždu. Kdykoli se takové myšlenky objeví, okamžitě kontaktujte svého lékaře.
Dávkování a způsob použití Jak používat Luminale: Dávkování
- LUMINALE® 200 mg / ml injekční roztok pro intramuskulární podání, 200 mg / ml INJEKČNÍ LAHVIČKY fenobarbitalu (ve formě sodné soli 219 mg): pokud lékař neurčí jinak, u dospělých jedna ampulka denně intramuskulárně. Nepřekračujte 400 mg za 24 hodin. U dětí 10 mg na každý rok od 1 roku.
- LUMINALE® 100 mg tablety: jako sedativum od 50 do 100 mg (polovina / jedna tableta) denně. Jako antikonvulzivum u dospělých od 100 do 300 mg (1-3 tablety) denně dvakrát - třikrát. U dětí by měly být dávky sníženy (ze 100 na 20 mg) podle věku a hmotnosti a je indikován přípravek Luminale ® 15 mg tablety.
Při těžké nespavosti 50 až 200 mg (půl až 2 tablety) večer, hodinu před spaním. Tablety lze rozpustit v malém množství vody nebo přidat do jídla. Při léčbě starších pacientů musí dávkování pečlivě stanovit lékař, který bude muset vyhodnotit možné snížení výše uvedených dávek.
Předávkování Co dělat, pokud jste užili příliš mnoho přípravku Luminale
Léčba akutní intoxikace barbituráty zahrnuje okamžitý výplach žaludku, pokud to stav pacienta umožňuje.
Odstranění již absorbovaného léčiva lze dosáhnout nucenou diurézou a alkalizací moči. V závažných případech je užitečná hemodialýza a může být nutné mechanicky kontrolovat dýchání. Aby se předešlo plicním komplikacím, je nutné podání antibiotik.
Nežádoucí účinky Jaké jsou vedlejší účinky Luminale
Kožní: vzácné kožní alergické projevy. Byly hlášeny vzácné případy multiformního erytému, Stevens-Johnsonova syndromu a toxické epidermální nekrolýzy (Lyellův syndrom).
Hepatobiliární: vzácné případy toxické hepatitidy.
Hematologické: vzácné případy leukopenie, agranulocytózy, trombocytopenie a purpury. U novorozenců matek léčených fenobarbitalem se může objevit hypotrombinemie reagující na léčbu vitamínem K. Během chronické léčby může dojít k megaloblastické anémii a osteomalácii citlivé na folát, které reagují na léčbu vitamínem D.
Centrální nervový systém: u některých subjektů se mohou vyskytovat zřídka: vzrušení, agitovanost a delirium. U pediatrických pacientů se mohou objevit projevy hyperaktivity. Po podání vysokých dávek může zejména u starších osob dojít k sedaci, ataxii, nystagmu a mentální zmatenosti.
Při používání přípravku Luminale byly hlášeny život ohrožující kožní vyrážky (Stevens-Johnsonův syndrom, toxická epidermální nekrolýza) .Frekvence: velmi vzácné
Byly hlášeny případy onemocnění kostí včetně osteopenie a osteoporózy (řídnutí kostí) a zlomenin. Kontaktujte svého lékaře nebo lékárníka, pokud dlouhodobě užíváte antiepileptická léčiva, nebo máte v anamnéze osteoporózu, nebo pokud užíváte steroidy.
Pacient je vyzván, aby oznámil ošetřujícímu lékaři možný výskyt nežádoucích účinků, které nejsou popsány.
Expirace a retence
Upozornění: přípravek nepoužívejte po uplynutí doby použitelnosti uvedené na obalu.
Složení
1 lahvička obsahuje:
Účinná látka: fenobarbital (ve formě sodné soli 219 mg) 200 mg.
Pomocné látky: propylenglykol, ethanol, voda na injekci.
1 tableta obsahuje:
Účinná látka: fenobarbital 100 mg.
Pomocné látky: mastek, povidon, kyselina stearová, kukuřičný škrob.
Léková forma
- Krabička s 10 ampulemi
- Balení 20 tablet
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Abyste měli přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
LUMINÁL
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
1 ampulka o objemu 1 ml obsahuje:
Účinná látka: FENOBARBITÁL (ve formě sodné soli 219 mg) 200 mg
1 tableta obsahuje 170 mg
Účinná látka: FENOBARBITAL 100 mg
03.0 LÉKOVÁ FORMA
- lahvičky
- tablety
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
LUMINALE je indikován především jako obecné sedativum, se zvláštním zřetelem na epilepsii a všechny stavy vyžadující dlouhotrvající sedaci. LUMINALE je zvláště užitečný při tonicko-klonických záchvatech grand mal a fokálních kortikálních záchvatů. LUMINALE lze také použít jako hypnotikum.
04.2 Dávkování a způsob podání
Luminale lahvičky
Není -li lékařem předepsáno jinak, 1 ampulka denně intramuskulárně u dospělých. Nepřekračujte 400 mg za 24 hodin.
U dětí 10 mg na každý rok věku počínaje 1. rokem.
Luminale 100 mg tablety
Jako sedativum 50 až 100 mg (1 / 2-1 tableta) denně.
Jako antikonvulzivum u dospělých od 100 do 300 mg (1-3 tablety) denně 2–3krát. U dětí by měly být dávky sníženy (z 20 na 100 mg) podle věku a hmotnosti a je indikován přípravek Luminale 15 mg tablety.
Při těžké nespavosti 50 až 200 mg (1/2 až 2 tablety) večer hodinu před spaním. Tablety lze rozpustit v malém množství vody nebo přidat do jídla. Při léčbě starších pacientů musí dávkování pečlivě stanovit lékař, který bude muset vyhodnotit možné snížení výše uvedených dávek.
04.3 Kontraindikace
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku tohoto přípravku.
Porfyrie, renální a jaterní insuficience, závažné srdeční choroby, akutní intoxikace alkoholem, analgetika, hypnotika.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Fenobarbital může být návykový. Pokračující terapie indukuje tvorbu jaterních enzymů, které urychlují metabolismus některých léků, jako jsou antikoagulancia, některá antibiotika, adrenální steroidy atd. Přípravky Hypericum perforatum by neměly být užívány současně s léčivými přípravky obsahujícími fenobarbital kvůli riziku snížení plazmatických hladin a snížené terapeutické účinnosti fenobarbitalu (viz bod 4.5 Interakce).
Účinek alkoholu je zvýšen a příjem alkoholických nápojů by měl být omezen Kombinace s jinými psychotropními léky a antihistaminiky vyžaduje zvláštní opatrnost a ostražitost lékaře, aby se předešlo neočekávaným nežádoucím účinkům interakce. Náhlé přerušení léčby u epileptických pacientů může vyvolat status epilepticus.
U pacientů užívajících antiepileptika v různých indikacích byly hlášeny případy sebevražedných představ a chování. Metaanalýza randomizovaných klinických studií versus placebo rovněž zdůraznila přítomnost mírného zvýšení rizika sebevražedných představ a chování.
Mechanismus tohoto rizika nebyl stanoven a dostupné údaje nevylučují možnost zvýšeného rizika u přípravku Luminale.
Pacienti by proto měli být sledováni z hlediska známek sebevražedných myšlenek a chování a v takovém případě by měla být zvážena vhodná léčba. Pacienti (a pečovatelé) by měli být poučeni, aby informovali svého ošetřujícího lékaře, pokud se objeví známky sebevražedných myšlenek nebo chování.
Při používání přípravku Luminale byly hlášeny následující život ohrožující kožní reakce: Stevens-Johnsonův syndrom (SJS) a toxická epidermální nekrolýza (TEN).
Pacienti by měli být informováni o známkách a příznacích a měli by být pečlivě sledováni z hlediska kožních reakcí. Nejvyšší riziko vzniku SJS a TEN se vyskytuje v prvních 8 týdnech léčby.
Pokud se objeví příznaky nebo příznaky SJS nebo TEN (např. Progresivní kožní vyrážka často s puchýři nebo slizničními lézemi), léčba přípravkem Luminale by měla být ukončena.
Nejlepší výsledky v managementu SJS a TEN jsou získány s včasnou diagnostikou a okamžitým přerušením léčby jakýmkoli podezřelým lékem.Včasné vysazení je spojeno s lepší prognózou.
Pokud se u pacienta vyvinul SJS nebo TEN pomocí Luminale, Luminale by již neměl být u tohoto pacienta znovu použit.
Uchovávejte mimo dosah a dohled dětí.
Viz také body 4.6 a 4.7.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Účinnost fenobarbitalu může být snížena současným podáváním přípravků na bázi Hypericum perforatum, což je způsobeno indukcí enzymů odpovědných za metabolismus léčiv přípravky na bázi Hypericum perforatum, které by proto neměly být podávány současně s fenobarbitalem. Indukční účinek může přetrvávat nejméně 2 týdny po ukončení léčby přípravky Hypericum perforatum. Pokud pacient současně užívá přípravky Hypericum perforatum, měly by být monitorovány hladiny fenobarbitalu v krvi a léčba přípravky Hypericum perforatum ukončena. Úroveň fenobarbitalu v krvi se může zvýšit zastavením Hypericum perforatum. Může být nutné upravit dávkování fenobarbitalu.
Viz bod 4.4
04.6 Těhotenství a kojení
Pacientkám, které mohou otěhotnět nebo jsou v plodném věku, by měla být poskytnuta odborná pomoc.
Pokud pacientka plánuje otěhotnět, měla by být přehodnocena potřeba antiepileptické léčby.
U potomků matek léčených antiepileptikem se riziko vrozených vad zvyšuje dvakrát až třikrát, nejčastěji hlášeným rozštěpem rtu, kardiovaskulárními malformacemi a vadami neurální trubice.
Polyterapie antiepileptiky může být spojena s vyšším rizikem vrozených vývojových vad než monoterapie. Proto je důležité, aby byla monoterapie praktikována, kdykoli je to možné.
Náhlé přerušení antiepileptické léčby by nemělo být prováděno kvůli nebezpečí obnovení záchvatů, které by mohly mít vážné důsledky pro matku i dítě.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Léčba fenobarbitalem snižuje pozornost a prodlužuje dobu reflexů: pacienti musí být na to upozorněni, aby se vyhnuli řízení vozidel nebo provádění operací, které kvůli své nebezpečnosti vyžadují integritu bdělosti.
04.8 Nežádoucí účinky
Kožní: vzácné kožní alergické projevy. Byly hlášeny vzácné případy multiformního erytému, Stevens-Johnsonova syndromu a toxické epidermální nekrolýzy (Lyellův syndrom).
Hepatobiliární: vzácné případy toxické hepatitidy.
Hematologické: vzácné případy leukopenie, agranulocytózy, trombocytopenie a purpury. U novorozenců matek léčených fenobarbitalem se může objevit hypotrombinemie reagující na léčbu vitamínem K.
Během chronické léčby může dojít k megaloblastické anémii a osteomalácii citlivé na folát, které reagují na léčbu vitamínem D.
Centrální nervový systém: u některých subjektů se mohou vyskytovat zřídka: vzrušení, agitovanost a delirium. U pediatrických pacientů se mohou objevit projevy hyperaktivity.
Po podání vysokých dávek může zejména u starších osob dojít k sedaci, ataxii, nystagmu a mentální zmatenosti.
Při používání přípravku Luminale byly hlášeny závažné kožní nežádoucí reakce (SCAR), jako je Steven-Johnosonův syndrom (SJS) a toxická epidermální nekrolýza (TEN)
Frekvence: velmi vzácné
U pacientů na dlouhodobé léčbě přípravkem Luminale byly hlášeny případy snížení minerální hustoty kostí, osteopenie, osteoporózy a zlomenin. Mechanismus, kterým Luminale ovlivňuje kostní metabolismus, nebyl identifikován.
Viz také body 4.4 - 4.6 a 4.7
04.9 Předávkování
Léčba akutní intoxikace barbituráty zahrnuje okamžitý výplach žaludku, pokud to podmínky pacienta umožňují. Odstranění již absorbovaného léčiva lze dosáhnout nucenou diurézou a alkalizací moči. V nejzávažnějších případech je užitečné uchýlit se k „hemodialýze a může být nutné mechanicky ovládat dýchání. Podávání antibiotik je nezbytné, aby se zabránilo vzniku plicních komplikací.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Fenobarbital je účinné hypnotikum-sedativum, které působí primárně na mozkovou kůru, zejména na motorická centra, zvyšuje práh excitability a také na neurovegetativní centra mozkového kmene. Má také spasmolytické vlastnosti, které umožňují jeho použití ve spastických stavech obecně.
05.2 Farmakokinetické vlastnosti
Orální absorpce fenobarbitalu je úplná, ale pomalá; vrcholové plazmatické koncentrace jsou stanoveny několik hodin po jednorázovém podání. Vazba na plazmatické bílkoviny je přibližně 40-60% a je také stejného řádu s jinými plazmatickými bílkovinami. Tkáněmi, včetně mozku. Distribuční objem je přibližně 0,9 1 / kg. Více než 25% fenobarbitalu je eliminováno renální exkrecí závislou na pH. Zbytkové množství je inaktivováno jaterními mikrozomálními enzymy. Hlavní metabolit, derivát parahydroxyfenylu, je neaktivní a je vylučován moč částečně jako sulfátový konjugát. Plazmatický poločas fenobarbitalu je u dospělých přibližně 90 hodin a u dětí o něco kratší.
05.3 Předklinické údaje vztahující se k bezpečnosti
Orální LD50 u potkanů je 660 mg / kg, což je více než 100násobek doporučené terapeutické dávky.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Luminale 200 mg injekční roztok pro intramuskulární podání
Pomocné látky: propylenglykol, ethanol, voda p.p.i.
Tablety Luminale
Pomocné látky: mastek, povidon, kyselina stearová, kukuřičný škrob
06.2 Neslučitelnost
Není známo.
06.3 Doba platnosti
Luminale 200 mg / ml injekční roztok pro intramuskulární podání:
Platnost: 2 roky.
Tablety Luminale
Platnost: 5 let.
06.4 Zvláštní opatření pro skladování
Chraňte před světlem.
Uvedené datum exspirace se vztahuje na produkt v neporušeném obalu, správně skladovaný.
06.5 Charakter vnitřního obalu a obsah balení
- 1 ml ampule: bezbarvé sklo typu I podle F.U. IX. Ed. Krabice s 10 lahvičkami
- Tablety: blistr (PVC-hliníkový spojený) neprůhledný. Balení 20 tablet
06.6 Návod k použití a zacházení
Nic k nahlášení.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
BRACCO S.p.A. přes E. Folli, 50 - Milán
08.0 REGISTRAČNÍ ČÍSLO
Luminale 200 mg / ml injekční roztok pro intramuskulární podání - AIC 002860017
Tablety Luminale - AIC 002860031
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
Luminale 200 mg / ml injekční roztok pro intramuskulární podání 12.07.1950 / 01.06.2005
Tablety Luminale - 16.10.1967 / 01.06.2010
10.0 DATUM REVIZE TEXTU
Červen 2012