Aktivní složky: Oxkarbazepin
TOLEP 300 mg tablety
TOLEP 600 mg tablety
Indikace Proč se používá tolep? K čemu to je?
Farmakoterapeutická skupina
Antiepileptikum, derivát karboxamidu.
Terapeutické indikace
Tolep je indikován k léčbě parciálních záchvatů s nebo bez sekundárních generalizovaných tonických klonických záchvatů.
Tolep je indikován k použití jak v monoterapii, tak v doplňkové terapii u dospělých a dětí ve věku 6 let a starších.
Kontraindikace Kdy by se tolep neměl používat
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku tohoto přípravku.
Opatření pro použití Co potřebujete vědět před užitím Tolepu
Tolep by měl být podáván pouze pod lékařským dohledem.
Přecitlivělost
V období po uvedení přípravku na trh byly hlášeny hypersenzitivní reakce třídy I (okamžité) včetně vyrážky, svědění, kopřivky, angioedému a případů anafylaxe. Po podání první nebo následujících dávek přípravku Tolep byly hlášeny případy anafylaxe a angioedému postihující hrtan, glottis, rty a oční víčka. Pokud se tyto reakce vyskytnou u pacienta po léčbě přípravkem Tolep, měl by podávání přípravku Tolep přerušit a měla by být zahájena alternativní léčba. zahájeno.
Pacienti, u kterých se vyskytly reakce z přecitlivělosti na karbamazepin, by měli být informováni, že přibližně u 25-30% stejných pacientů se mohou po užití přípravku Tolep znovu objevit podobné reakce (např. Závažné kožní reakce) (viz „Nežádoucí účinky“).
Hypersenzitivní reakce, včetně multiorgánových hypersenzitivních reakcí, se mohou objevit také u pacientů, kteří neměli předchozí epizody přecitlivělosti na karbamazepin. Tyto reakce mohou postihnout kůži, játra, krev a lymfatický systém nebo jiné orgány, a to jednotlivě nebo současně v případě systémové reakce (viz „Nežádoucí účinky“). Obecně platí, že pokud se objeví známky a příznaky naznačující reakce přecitlivělosti, podávání Tolepu by mělo být okamžitě zastaveno.
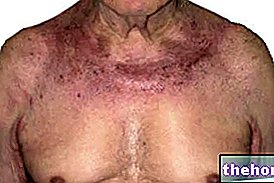
Dermatologické účinky
Ve velmi vzácných případech byly v souvislosti s používáním přípravku Tolep hlášeny závažné dermatologické reakce, včetně Stevens-Johnsonova syndromu, toxické epidermální nekrolýzy (Lyellův syndrom) a multiformního erytému. Pacienti s těžkými dermatologickými reakcemi mohou potřebovat hospitalizaci, protože tyto stavy mohou být život ohrožující a velmi vzácně smrtelné.Epizody tohoto typu spojené s používáním Tolepu byly hlášeny u dětí i dospělých. Průměrná doba nástupu byla 19 dní. Po zahájení léčby přípravkem Tolep bylo hlášeno několik ojedinělých případů recidivy závažných kožních reakcí. Pacienti na terapii Tolepem, u kterých se objeví kožní reakce, by měli být okamžitě vyšetřeni a léčba Tolepem by měla být okamžitě ukončena, pokud vyrážka zjevně nesouvisí s léčivem. Pokud je léčba ukončena, mělo by být zváženo nahrazení Tolepu jiným antiepileptickým léčivým přípravkem, aby se zabránilo záchvatům z vysazení.Tolep nesmí být znovu podáván pacientům, kteří přerušili léčbu kvůli reakcím z přecitlivělosti (viz „Kontraindikace“).
Riziko závažných kožních reakcí u čínských nebo thajských pacientů spojených s karbamazepinem nebo chemicky příbuznými látkami lze předvídat testováním vzorku krve od těchto pacientů. Váš lékař by měl být schopen poradit, zda je před podáním oxkarbazepinu nutné provést krevní testy.
Riziko zhoršení záchvatů
Během léčby oxkarbazepinem bylo hlášeno riziko zhoršení záchvatů. Riziko zhoršení záchvatů bylo pozorováno hlavně u dětí, ale může se vyskytnout i u dospělých. V případě zhoršení záchvatů by měla být léčba přípravkem Tolep přerušena.
Hyponatrémie
U pacientů s již existující renální dysfunkcí spojenou s nízkými hladinami sodíku (např. Syndrom nepřiměřené sekrece ADH) nebo u pacientů léčených souběžně léky snižujícími hladinu sodíku (např. Diuretiky, desmopresinem, molekulami spojenými s nepřiměřenou sekrecí ADH) jako u nesteroidních protizánětlivé léky (např. indomethacin), hladiny sodíku v krvi by měly být měřeny před zahájením léčby, přibližně po dvou týdnech a poté v měsíčních intervalech během prvních tří měsíců léčby, nebo podle posouzení lékaře. Tyto rizikové faktory mohou postihnout hlavně starší pacienty. Pacienti, kteří již užívají přípravek Tolep a kteří zahájí léčbu léky snižujícími hladinu sodíku, by měli podstoupit stejné kontroly hladin sodíku v krvi. Obecně platí, že pokud se během léčby přípravkem Tolep objeví příznaky naznačující hyponatrémii (příliš nízké hladiny sodíku v krvi; viz „Nežádoucí účinky“), může se lékař rozhodnout provést měření sodíku v krvi. U ostatních pacientů mohou být tyto testy součástí běžných laboratorních kontrol.
Všem pacientům se srdečním selháním a sekundárním srdečním selháním by měla být pravidelně kontrolována váha, aby se ujistil, že nedochází k zadržování tekutin. V případě zadržování tekutin nebo zhoršení srdečních stavů by měla být zkontrolována hladina sodíku v krvi. Pokud je pozorována hyponatrémie, může být užitečné snížit množství přijímaných tekutin. Pacienti s již existujícími poruchami vedení (např. Atrioventrikulární blok, arytmie) by měli být pečlivě sledováni.
Hypotyreóza
Hypotyreóza je velmi vzácná nežádoucí reakce na oxkarbazepin. Vzhledem k významu hormonů štítné žlázy pro vývoj dětí po narození se doporučuje před zahájením léčby Tolepem u dětských pacientů zkontrolovat funkci štítné žlázy. U dětských pacientů se během léčby Tolepem doporučuje sledování funkce štítné žlázy.
Funkce jater
Byly hlášeny velmi vzácné epizody hepatitidy, které ve většině případů příznivě odezněly. Pokud je podezření na jaterní účinek, je třeba sledovat jaterní funkce a zvážit přerušení léčby přípravkem Tolep.Při podávání přípravku Tolep pacientům s těžkou poruchou funkce jater je nutná opatrnost (viz „Dávka, způsob a načasování podávání“).
Funkce ledvin
U pacientů s poruchou funkce ledvin (clearance kreatininu nižší než 30 ml / min) je během léčby přípravkem Tolep třeba opatrnosti, zejména s ohledem na počáteční dávku a titraci dávky (viz „Dávka, způsob a doba podání“).
Hematologické účinky
Po uvedení na trh byly u pacientů léčených přípravkem Tolep hlášeny velmi vzácné případy agranulocytózy, aplastické anémie a pancytopenie (viz „Nežádoucí účinky“). Pokud se objeví známky výrazného útlumu kostní dřeně, je třeba zvážit přerušení léčby.
Hormonální antikoncepce
Pacientky ve fertilním věku by měly být poučeny o tom, že souběžné používání přípravku Tolep a hormonální antikoncepce může jeho účinek zrušit (viz „Interakce“). Během léčby Tolepem se doporučuje používat alternativní nehormonální antikoncepční metody.
Alkohol
Extrémní opatrnost je vyžadována při konzumaci alkoholických nápojů během užívání Tolepu kvůli možnému aditivnímu sedativnímu účinku.
Sebevražedné myšlenky a chování
U malého počtu pacientů léčených antiepileptiky, jako je Tolep, se objevily myšlenky na sebepoškozování nebo sebevraždu. Kdykoli se takové myšlenky objeví, okamžitě kontaktujte svého lékaře.
Přerušení léčby
Stejně jako u jiných antiepileptik by léčba přípravkem Tolep měla být ukončena postupně, aby se minimalizovalo riziko zvýšené frekvence záchvatů.
Interakce Které léky nebo potraviny mohou ovlivnit účinek Tolepu
Informujte svého lékaře nebo lékárníka o všech lécích, které užíváte nebo jste v nedávné době užíval, a to i o lécích, které jsou dostupné bez lékařského předpisu.
Byly pozorovány potenciální interakce mezi přípravkem Tolep a jinými antiepileptiky, jako je karbamazepin, fenobarbital, fenytoin, kyselina valproová a lamotrigin. Pokud je současně s oxkarbazepinem podáváno jedno nebo více antiepileptik, může být podle potřeby nutná opatrná úprava dávky a / nebo monitorování plazmatických hladin, zvláště u pediatrických pacientů souběžně léčených lamotriginem. Souběžná léčba přípravkem Tolep a lamotriginu byla spojena se zvýšeným rizikem nežádoucích účinků (nauzea, somnolence, závratě a bolesti hlavy).
Bylo prokázáno, že tolep ovlivňuje dvě složky perorální antikoncepce, ethinylestradiol a levonorgestrel. Proto může současné užívání tolepu a hormonální antikoncepce způsobit, že tyto přípravky budou neúčinné (viz „Opatření pro použití“). Jiné metody antikoncepce, jiné než hormonální , je třeba vzít v úvahu.
Interakce mezi Tolepem a imunosupresivy (např. Cyklosporin, takrolimus) jsou možné.
Interakce mezi oxkarbazepinem a inhibitory MAO je teoreticky možná na základě strukturálního vztahu mezi oxkarbazepinem a tricyklickými antidepresivy. Do klinických studií byli zařazeni pacienti na tricyklických antidepresivech a nebyly pozorovány žádné klinicky významné interakce. Podávání oxkarbazepinu a lithium může způsobit zvýšenou neurotoxicitu.
Po přerušení léčby přípravkem Tolep může být po příslušném klinickém hodnocení a / nebo monitorování plazmatické hladiny nutné snížení dávky souběžně podávaných léčivých přípravků.
Bylo prokázáno, že tolep neinterferuje s warfarinem, viloxazinem, cimetidinem, erythromycinem a dextropropoxyfenem.
Varování Je důležité vědět, že:
Těhotenství
Před užitím jakéhokoli léku se poraďte se svým lékařem nebo lékárníkem. Rizika spojená s epilepsií a antiepileptiky obecně Pacientům, kteří mohou otěhotnět nebo jsou v plodném věku, by měla být poskytnuta odborná pomoc.
Pokud pacientka plánuje otěhotnět, měla by být přehodnocena potřeba antiepileptické léčby.
Bylo prokázáno, že výskyt malformací je dvakrát až třikrát vyšší u osob narozených ženám s epilepsií než s frekvencí přibližně 3% v běžné populaci.
O těch, které se narodily epileptickým ženám, je známo, že jsou náchylnější k vývojovým poruchám, včetně malformací. Údaje z omezeného počtu těhotenství naznačují, že oxkarbazepin může při podávání během těhotenství způsobit vážné vrozené vady.
U léčené populace byl pozorován nárůst malformací s polyterapií, nebylo však objasněno, do jaké míry je za onemocnění zodpovědná léčba. Účinná antiepileptická terapie by navíc neměla být přerušována, protože zhoršení onemocnění je škodlivé jak pro matku, tak pro plod.
Vezmeme -li v úvahu toto vše:
- Pokud pacientky užívající přípravek Tolep otěhotní nebo plánují otěhotnět, nebo pokud potřebují zahájit léčbu přípravkem Tolep v průběhu těhotenství, je třeba potenciální přínosy tohoto léku pečlivě zvážit oproti potenciálnímu riziku malformací plodu. To je zvláště důležité během prvních tří měsíců těhotenství.
- Je třeba podávat nejnižší účinné dávky.
- U žen ve fertilním věku by měl být přípravek Tolep podáván jako monoterapie, kdykoli je to možné.
- Pacienti by měli být upozorněni, že se může zvýšit riziko malformací, a měli by být schopni podstoupit prenatální screening.
- Během těhotenství by neměla být účinná antiepileptická léčba oxkarbazepinem přerušena, protože zhoršení onemocnění je škodlivé jak pro matku, tak pro plod.
Monitorování a prevence
Antiepileptika mohou přispět k nedostatku kyseliny listové, což je jeden z možných faktorů odpovědných za abnormality plodu. Před a během těhotenství se doporučuje doplňkové podávání kyseliny listové. Vzhledem k tomu, že účinnost tohoto doplňkového podávání není prokázána, je možné u žen na doplňkové léčbě kyselinou listovou uvažovat o vhodnosti specifické prenatální diagnostiky.
V důsledku fyziologických změn, ke kterým dochází, se mohou plazmatické hladiny aktivního metabolitu oxkarbazepinu (monohydroxylovaného derivátu, MHD) během těhotenství postupně snižovat. Proto se u žen podstupujících léčbu Tolepem během těhotenství doporučuje pečlivě sledovat klinickou odpověď a zvážit sledování plazmatických koncentrací MHD, aby byla zajištěna adekvátní kontrola záchvatů během těhotenství. Po porodu lze také zvážit sledování plazmatických koncentrací MHD, zvláště pokud byly dávky léčiva během těhotenství zvýšeny.
U novorozence
U novorozenců byly hlášeny poruchy krvácení způsobené antiepileptiky. Preventivně by měl být vitamín K1 podáván k preventivním účelům v posledních týdnech těhotenství a následně novorozencům.
Čas krmení
Oxkarbazepin a jeho aktivní metabolit (MHD) se vylučují do mateřského mléka. Účinky na kojence vystavené tímto způsobem Tolep nejsou známy. Tolep by proto neměl být užíván během kojení.
Ženy v plodném věku a antikoncepční opatření
Ženy ve fertilním věku by měly být poučeny o nutnosti používání vysoce účinných metod antikoncepce (nejlépe nehormonálních, jako jsou nitroděložní implantáty) během léčby přípravkem Tolep. Užívání Tolepu může zrušit terapeutický účinek perorálních kontraceptiv na bázi ethinylestradiolu a levonorgestrelu (viz „Interakce“ a „Opatření pro použití“).
Plodnost
Nejsou k dispozici žádné údaje o fertilitě u lidí.
Účinky na schopnost řídit a obsluhovat stroje
Při užívání oxkarbazepinu byly hlášeny nežádoucí účinky, jako jsou závratě, somnolence, ataxie, diplopie, rozmazané vidění, poruchy vidění, hyponatrémie, poruchy vědomí (úplný seznam nežádoucích účinků viz „Nežádoucí účinky“), zejména na začátku léčby nebo při úpravách dávky (častěji během fáze titrace) .Pacienti by proto měli být při řízení a obsluze strojů obezřetní.
Dávkování a způsob použití Jak používat Tolep: Dávkování
Jako monoterapie a jako doplňková terapie by léčba přípravkem Tolep měla být zahájena podáním klinicky účinné dávky rozdělené do dvou podání. Dávku lze zvýšit podle klinické odpovědi pacienta. Pokud je přípravek Tolep používán jako náhrada jiných antiepileptických léčivých přípravků, dávka kombinovaných antiepileptických léčivých přípravků by měla být při zahájení léčby přípravkem Tolep postupně snižována. Při doplňkové terapii, protože se celková zátěž antiepileptických léčivých přípravků na pacienta zvyšuje, může být nutné snížit dávku jiných kombinovaných antiepileptik a / nebo zvýšit dávku Tolepu pomaleji (viz bod „Opatření pro použití").
Dospělí
Monoterapie
Doporučená počáteční dávka
Léčba přípravkem Tolep by měla začít dávkou 600 mg / den (8-10 mg / kg / den) rozdělenou do dvou dávek.
Udržovací dávka
Pokud je to klinicky indikováno, lze dávku zvyšovat v maximálních přírůstcích 600 mg / den v přibližně týdenních intervalech od počáteční dávky, dokud není dosaženo požadované klinické odpovědi. Terapeutické účinky jsou pozorovány při dávkách mezi 600 mg / den a 2400 mg / den.
Maximální doporučená dávka
V kontrolovaném nemocničním prostředí bylo během 48 hodin dosaženo zvýšení dávky až na 2 400 mg / den.
Doplňková terapie
Doporučená počáteční dávka
Léčba přípravkem Tolep by měla začít dávkou 600 mg / den (8-10 mg / kg / den) rozdělenou do dvou dávek.
Udržovací dávka
Pokud je to klinicky indikováno, lze dávku zvyšovat v maximálních přírůstcích 600 mg / den v přibližně týdenních intervalech počínaje počáteční dávkou, dokud není dosaženo požadované klinické odpovědi. Terapeutické účinky jsou pozorovány při dávkách mezi 600 mg / den a 2400 mg / den.
Maximální doporučená dávka
Účinné byly denní dávky v rozmezí od 600 do 2 400 mg / den, ačkoli většina pacientů nebyla schopna tolerovat dávku 2 400 mg / den bez souběžného snížení dalších antiepileptických léčivých přípravků, zejména kvůli výskytu nežádoucích účinků spojených s léčivem. Nervový systém. Denní dávky nad 2400 mg / den nebyly v klinických studiích systematicky hodnoceny.
Starší pacienti (65 let nebo starší)
U starších pacientů nejsou nutná žádná zvláštní doporučení pro dávkování, protože terapeutické dávky se upravují individuálně. U starších pacientů s poruchou funkce ledvin (clearance kreatininu nižší než 30 ml / min) se doporučuje úprava dávkování (viz bod „Pacienti s poruchou funkce ledvin“). U pacientů s rizikem hyponatrémie se doporučuje pečlivé sledování hladin sodíku (viz „Opatření pro použití“).
Pacienti s poruchou funkce jater
U pacientů s lehkou až středně těžkou poruchou funkce jater není nutná úprava dávkování. Tolep nebyl studován u pacientů s těžkou poruchou funkce jater, proto se při podávání přípravku Tolep těmto pacientům doporučuje opatrnost.
Pacienti s poruchou funkce ledvin
U pacientů s poruchou funkce ledvin (clearance kreatininu nižší než 30 ml / min) by měla být léčba přípravkem Tolep zahájena poloviční obvyklou počáteční dávkou (300 mg / den) a zvyšována alespoň v týdenních intervalech, dokud není dosaženo požadované klinické odpovědi (viz „Opatření pro použijte “). Zvýšení dávky u pacientů s poruchou funkce ledvin může vyžadovat bližší sledování.
Děti
Doporučená počáteční dávka
Jako monoterapie a jako doplňková terapie by léčba přípravkem Tolep měla začínat dávkou 8–10 mg / kg / den rozdělenou do dvou podání.
Udržovací dávka
Udržovací dávka 30-46 mg / kg / den, dosahovaná po dobu dvou týdnů, byla prokázána jako účinná a dobře tolerovaná u dětí. Terapeutické účinky byly pozorovány při průměrné udržovací dávce přibližně 30 mg / kg. / Den.
Maximální doporučená dávka
Pokud je to klinicky indikováno, lze dávku zvýšit v maximálních přírůstcích po 10 mg / kg / den v přibližně týdenních intervalech počínaje počáteční dávkou až po maximální dávku 46 mg / kg / den, aby se dosáhlo požadované klinické odpovědi.
Tolep je indikován k použití u dětí ve věku 6 let a starších.U dětí mladších 6 let se tolep nedoporučuje, protože bezpečnost a účinnost nebyla dostatečně prokázána.
Všechna výše popsaná doporučení (dospělí, starší lidé a děti) se týkají dávek studovaných v klinických studiích u všech věkových skupin. Může však být rozhodnuto, pokud je to vhodné, zahájit léčbu nižšími dávkami.
Způsob podání
Tablety mají půlicí rýhu a lze je rozdělit na polovinu, aby se snáze polykaly. Tabletu však nelze rozdělit na stejné dávky.
Tolep lze užívat s jídlem nebo bez jídla.
Terapeutické monitorování
Terapeutický účinek oxkarbazepinu se projevuje především prostřednictvím jeho aktivního metabolitu 10-monohydroxyderivátu (MHD). Rutinní monitorování hladin oxkarbazepinu nebo MHD v plazmě není opodstatněné. Monitorování plazmatických hladin MHD však lze vzít v úvahu. vyloučit nedodržení léčby nebo v situacích, kdy lze očekávat změnu clearance MHD, včetně následujících:
- změny funkce ledvin (viz „Pacienti s poruchou funkce ledvin“)
- těhotenství (viz „Zvláštní upozornění - těhotenství“)
- současné užívání léčivých přípravků, které mají indukční účinek na jaterní enzymy (viz „Interakce“).
- dětského a geriatrického věku
Pokud nastane některá z těchto situací, lze dávku přípravku Tolep upravit (na základě plazmatických hladin naměřených 2–4 hodiny po podání dávky) tak, aby byly maximální plazmatické hladiny MHD <35 mg / l.
Předávkování Co dělat, když jste užil příliš mnoho Tolepu
Byly hlášeny ojedinělé případy předávkování. Maximální užitá dávka byla přibližně 24 000 mg.
Příznaky a symptomy
Bilance hydro-elektrolytů: hyponatrémie
Oční poruchy: diplopie, mióza, rozmazané vidění
Gastrointestinální poruchy: nevolnost, zvracení, hyperkineze
Celkové poruchy a reakce v místě aplikace: astenie
Vyšetřování: deprese dechové frekvence, prodloužení QTc intervalu
Poruchy nervového systému: ospalost a ospalost, závratě, ataxie, nystagmus, třes, poruchy koordinace (abnormální koordinace), křeče, bolesti hlavy, kóma, bezvědomí, dyskineze
Psychiatrické poruchy: agresivita, agitovanost, stav zmatenosti
Cévní poruchy: hypotenze
Respirační, hrudní a mediastinální poruchy: dušnost.
Léčba
Neexistuje žádné specifické antidotum. Pacienti s příznaky otravy v důsledku předávkování Tolepem by měli být léčeni vhodnou symptomatickou a podpůrnou terapií a lék by měl být volitelně odstraněn výplachem žaludku nebo inaktivován podáním aktivního uhlí.
V případě náhodného požití / požití nadměrné dávky Tolepu okamžitě informujte svého lékaře nebo jděte do nejbližší nemocnice.
Nežádoucí účinky Jaké jsou vedlejší účinky přípravku Tolep
Podobně jako všechny léky, může mít i Tolep nežádoucí účinky, které se ale nemusí vyskytnout u každého.
Nejčastěji hlášenými nežádoucími účinky jsou somnolence, bolest hlavy, závratě, diplopie, nauzea, zvracení a únava, které se vyskytly u více než 10% pacientů.
Nežádoucí účinky jsou uvedeny níže rozdělené podle typu a frekvence. V každé frekvenční třídě jsou nežádoucí účinky hlášeny sestupně podle závažnosti.
Poruchy krve a lymfatického systému
- Méně časté: leukopenie.
- Velmi vzácné: trombocytopenie
- Není známo: deprese kostní dřeně, aplastická anémie, agranulocytóza, pancytopenie, neutropenie.
Poruchy imunitního systému
- Velmi vzácné: přecitlivělost (včetně přecitlivělosti na více orgánů) charakterizovaná vyrážkou, horečkou. Postiženy mohou být i jiné orgány nebo systémy, například krev a lymfatický systém (např. Eozinofilie, trombocytopenie, leukopenie, lymfadenopatie, splenomegalie), játra (např. Abnormální výsledky testů jaterních funkcí, hepatitida), svaly a klouby (např. Otoky kloubů, myalgie) , artralgie), nervový systém (např. jaterní encefalopatie), ledviny (např. proteinurie, intersticiální nefritida, selhání ledvin), plíce (např. dušnost, plicní edém, astma, bronchospasmus, intersticiální plicní onemocnění), angioedém.
- Není známo: anafylaktické reakce.
Endokrinní patologie
- Není známo: hypotyreóza.
Poruchy metabolismu a výživy
- Časté: hyponatrémie.
- Velmi vzácné: Hyponatrémie * spojená se známkami a příznaky, jako jsou záchvaty, zmatenost, změna vědomí, encefalopatie, poruchy vidění (např. Rozmazané vidění), zvracení, nauzea, nedostatek kyseliny listové
Psychiatrické poruchy
- Časté: stav zmatenosti, deprese, apatie, agitovanost (např. Nervozita), emoční křehkost.
Poruchy nervového systému
- Velmi časté: somnolence, bolest hlavy, závratě.
- Časté: ataxie, třes, nystagmus, narušená koncentrace, amnézie.
Oční poruchy
- Velmi časté: diplopie.
- Časté: rozmazané vidění, poruchy vidění.
Poruchy ucha a labyrintu
- Časté: závratě
Srdeční patologie
- Velmi vzácné: arytmie, atrioventrikulární blok.
Cévní patologie
- Není známo: hypertenze.
Gastrointestinální poruchy
- Velmi časté: nevolnost, zvracení.
- Časté: průjem, zácpa, bolest břicha.
- Velmi vzácné: pankreatitida a / nebo zvýšená lipáza a / nebo amyláza
Poruchy jater a žlučových cest
- Velmi vzácné: hepatitida.
Poruchy kůže a podkožní tkáně
- Časté: vyrážka, alopecie, akné.
- Méně časté: kopřivka.
- Velmi vzácné: angioedém, Stevens-Johnsonův syndrom, toxická epidermální nekrolýza (Lyellův syndrom), multiformní erytém (viz „Opatření pro použití“).
Poruchy svalové a kosterní soustavy a pojivové tkáně
- Velmi vzácné: systémový lupus erythematodes
Celkové poruchy a reakce v místě aplikace
- Velmi časté: únava. - Časté: astenie.
Diagnostické testy
- Méně časté: zvýšené hodnoty jaterních enzymů, zvýšené hodnoty alkalické fosfatázy v krvi.
- Velmi vzácné: zvýšení hodnot amylázy, zvýšení hodnot lipázy.
- Není známo: pokles hladin T4
* Klinicky významná hyponatrémie (sodná sůl sodíku v séru
Nežádoucí účinky ze spontánních hlášení a literatury (frekvence není známa)
Následující nežádoucí účinky pocházejí z postmarketingových zkušeností s přípravkem Tolep a odkazují na spontánní hlášení a případy popsané v literatuře. Protože tyto reakce vznikají spontánně z populace nejisté velikosti, není možné s jistotou odhadnout frekvenci, která je proto indikována. ... jako „není známo“. Nežádoucí účinky jsou seřazeny podle tříd orgánových systémů MedDRA. V každé třídě jsou nežádoucí účinky seřazeny podle klesající závažnosti.
Poruchy imunitního systému
Drogová vyrážka s eozinofilií a systémovými příznaky (DRESS).
Poruchy metabolismu a výživy
Syndrom nepřiměřené sekrece ADH se známkami a příznaky, jako je letargie, nevolnost, závratě, snížená osmolalita séra (krve), zvracení, bolest hlavy, zmatenost nebo jiné neurologické příznaky a symptomy.
Poruchy kůže a podkožní tkáně
Akutní generalizovaná exantematózní pustulóza (AGEP).
Zranění, otravy a procedurální komplikace
Pády.
Poruchy nervového systému
Poruchy řeči (včetně dysartrie), častější během fáze titrace. Poruchy svalové a kosterní soustavy a pojivové tkáně Byly hlášeny případy onemocnění kostí včetně osteopenie a osteoporózy (řídnutí kostí) a zlomenin. Kontaktujte svého lékaře nebo lékárníka, pokud dlouhodobě užíváte antiepileptická léčiva, nebo máte v anamnéze osteoporózu, nebo pokud užíváte steroidy.
Dodržování pokynů obsažených v příbalové informaci snižuje riziko nežádoucích účinků.
Hlášení nežádoucích účinků
Pokud se u vás vyskytne kterýkoli z nežádoucích účinků, sdělte to svému lékaři nebo lékárníkovi. Nežádoucí účinky můžete hlásit také přímo na adresu: Státní ústav pro kontrolu léčiv Šrobárova 48100 41 Praha 10 Webové stránky: www.sukl.cz/nahlasit-nezadouci-ucinek Nahlášením nežádoucích účinků můžete přispět k získání více informací o bezpečnosti tohoto přípravku.
Expirace a retence
Expirace: viz datum spotřeby vytištěné na obalu
Doba použitelnosti se vztahuje na výrobek v neporušeném a správně skladovaném obalu.
Upozornění: přípravek nepoužívejte po uplynutí doby použitelnosti uvedené na obalu
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
Léčivé přípravky se nesmí vyhazovat do odpadních vod nebo domácího odpadu. Zeptejte se svého lékárníka, jak naložit s přípravky, které již nepoužíváte. Pomůže to chránit životní prostředí.
Uchovávejte tento přípravek mimo dohled a dosah dětí
Složení a léková forma
Složení
Jedna 300 mg dělitelná tableta obsahuje: 300 mg oxkarbazepinu.
Jedna 600 mg dělitelná tableta obsahuje: 600 mg oxkarbazepinu.
Pomocné látky: koloidní bezvodý oxid křemičitý; mikrokrystalická celulóza; hypromelóza; červený oxid železitý; žlutý oxid železitý; stearát hořečnatý; sodná sůl karmelózy
Léková forma a obsah
Tablety
Krabička s 50 dělitelnými tabletami po 300 mg.
Krabička s 50 dělitelnými tabletami po 600 mg.
Zdroj příbalové informace: AIFA (Italská agentura pro léčivé přípravky). Obsah zveřejněný v lednu 2016. Přítomné informace nemusí být aktuální.
Chcete-li mít přístup k nejaktuálnější verzi, doporučujeme navštívit webovou stránku AIFA (Italská agentura pro léčivé přípravky). Prohlášení a užitečné informace.
01.0 NÁZEV LÉČIVÉHO PŘÍPRAVKU
TOLEPOVÉ TABLETY
02.0 KVALITATIVNÍ A KVANTITATIVNÍ SLOŽENÍ
Jedna 300 mg dělitelná tableta obsahuje:
Oxkarbazepin 300 mg
Jedna 600 mg dělitelná tableta obsahuje:
Oxkarbazepin 600 mg
Úplný seznam pomocných látek viz bod 6.1.
03.0 LÉKOVÁ FORMA
Tablety.
04.0 KLINICKÉ INFORMACE
04.1 Terapeutické indikace
Epilepsie
- částečné záchvaty se sekundární generalizací nebo bez ní
- generalizované tonicko-klonické záchvaty.
04.2 Dávkování a způsob podání
Dávkování
Léčba přípravkem Tolep, ať už je podávána jako mono nebo polyfarmace, by měla být zahájena postupně a dávkování by mělo být přizpůsobeno potřebám konkrétního pacienta.
Dospělí
Monoterapie: doporučená počáteční dávka je 300 mg denně, dávku lze postupně zvyšovat, dokud není dosaženo nejlepší odpovědi, obvykle kolem 600-1200 mg / den.
Polyterapie (u pacientů s nedostatečně kontrolovanou epilepsií nebo v případech refrakterních na terapii): doporučená počáteční dávka je 300 mg denně, dávku lze postupně zvyšovat, dokud není dosaženo nejlepší odpovědi Udržovací dávka se pohybuje mezi 900 a 3000 mg / den.
Děti
Zkušenosti s přípravkem Tolep u dětí jsou omezené a u dětí mladších 3 let nejsou žádné zkušenosti.
Kromě toho, protože je obtížné přizpůsobit dávkování dostupnými tabletami a rozdělit denní dávku na 2–3krát, používání Tolepu v dětském věku se nedoporučuje. Použití přípravku u dětí mladších 3 let se však nedoporučuje je třeba se vyhnout.
Pacienti s jaterní insuficiencí
U pacientů s lehkou až středně těžkou poruchou funkce jater není nutná úprava dávkování. Tolep nebyl studován u pacientů s těžkou poruchou funkce jater, proto se při podávání přípravku Tolep těmto pacientům doporučuje opatrnost.
Pacienti s renální insuficiencí
U pacientů s renální insuficiencí (clearance kreatininu nižší než 30 ml / min) by měla být dávka přípravku Tolep pečlivě stanovena a dávka by měla být zvyšována nejméně jednou týdně, dokud nebude dosaženo požadované klinické odpovědi.
Správa
Tolep by měl být podáván třikrát denně, ale pokud je to možné, měl by být podáván dvakrát denně. Tablety lze užívat během jídla nebo po jídle a zapít trochou tekutiny.
04.3 Kontraindikace
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku tohoto přípravku.
04.4 Zvláštní upozornění a vhodná opatření pro použití
Přecitlivělost
V období po uvedení přípravku na trh byly hlášeny hypersenzitivní reakce třídy I (okamžité) včetně vyrážky, svědění, kopřivky, angioedému a případů anafylaxe. Po podání první nebo následujících dávek přípravku Tolep byly hlášeny případy anafylaxe a angioedému postihující hrtan, glottis, rty a oční víčka. Pokud se tyto reakce vyskytnou u pacienta po léčbě přípravkem Tolep, měl by podávání přípravku Tolep přerušit a měla by být zahájena alternativní léčba. zahájeno.
Pacienti, u kterých se vyskytly reakce z přecitlivělosti na karbamazepin, by měli být informováni, že přibližně u 25-30% stejných pacientů se mohou po užití přípravku Tolep objevit podobné reakce (např. Závažné kožní reakce) (viz bod 4.8).
Hypersenzitivní reakce, včetně multiorgánových hypersenzitivních reakcí, se mohou objevit také u pacientů, kteří neměli předchozí epizody přecitlivělosti na karbamazepin. Tyto reakce mohou postihnout kůži, játra, krev a lymfatický systém nebo jiné orgány, jednotlivě nebo současně v případě systémové reakce (viz bod 4.8). Obecně platí, že pokud se objeví známky a příznaky naznačující reakce přecitlivělosti, podávání Tolepu by mělo být okamžitě zastaveno.
Dermatologické účinky
Ve velmi vzácných případech byly v souvislosti s používáním přípravku Tolep hlášeny závažné dermatologické reakce, včetně Stevens-Johnsonova syndromu, toxické epidermální nekrolýzy (Lyellův syndrom) a multiformního erytému. Pacienti s těžkými dermatologickými reakcemi mohou potřebovat hospitalizaci, protože tyto stavy mohou být život ohrožující a velmi vzácně smrtelné.Epizody tohoto typu spojené s používáním Tolepu byly hlášeny u dětí i dospělých. Průměrná doba nástupu byla 19 dní. Po zahájení léčby přípravkem Tolep bylo hlášeno několik ojedinělých případů recidivy závažných kožních reakcí. Pacienti na terapii Tolepem, u kterých se objeví kožní reakce, by měli být okamžitě vyšetřeni a léčba Tolepem by měla být okamžitě ukončena, pokud vyrážka zjevně nesouvisí s léčivem. Pokud je léčba ukončena, mělo by být zváženo nahrazení Tolepu jiným antiepileptickým léčivým přípravkem, aby se zabránilo záchvatům z vysazení.Tolep nesmí být znovu podáván pacientům, kteří přerušili léčbu kvůli reakcím z přecitlivělosti (viz bod 4.3).
Allele HLA -B * 1502 - v čínské populaci hanského etnika, thajské a jiné asijské populace
U jedinců čínského původu etnické příslušnosti Han a thajského původu bylo prokázáno, že pozitivita na alelu HLA-B * 1502 je silně spojena s rizikem vzniku závažných kožních reakcí, jako je Steven-Johnsonův syndrom (SJS) během léčby karbamazepinem Chemická struktura oxkarbazepinu je podobná jako u karbamazepinu a je možné, že u pacientů pozitivních na HLA-B * 1502 může být také riziko rozvoje SJS po léčbě oxkarbazepinem. Některá data naznačují, že taková asociace existuje. oxkarbazepin Prevalence nosičů alely HLA-B * 1502 je v čínské populaci Han a Thajska asi 10%. V Koreji a Indii byly hlášeny alelické frekvence až asi 2% a 6%.
Pokud je to možné, měli by být tito jedinci vyšetřeni na tuto alelu před zahájením léčby karbamazepinem nebo chemicky příbuznými látkami. Pokud je u pacientů tohoto původu pozitivní test na alelu HLA-B * 1502, lze použití Tolepu zvážit pouze tehdy, pokud očekávané přínosy převažují nad riziky.
Vzhledem k prevalenci této alely v jiných asijských populacích (např. Nad 15% na Filipínách a v Malajsii) lze zvážit testování geneticky rizikových populací na přítomnost alely HLA-B * 1502.
Prevalence alely HLA-B * 1502 je zanedbatelná, například v populacích evropského původu, Afriky, v hispánském populačním vzorku a v japonštině (
Přítomnost alely HLA-B * 1502 může být rizikovým faktorem pro rozvoj SJS / TEN u čínských pacientů užívajících jiná antiepileptika, která mohou způsobit SJS / TEN. Proto u pacientů pozitivních na alelu HLA-B. * 1502 Je třeba dbát na to, aby se zabránilo užívání jiných léků, které mohou způsobit SJS / TEN.
Allele HLA -A * 3101 - v populaci evropského původu a v japonské populaci
Některá data naznačují, že alela HLA-A * 3101 je spojena se zvýšeným rizikem karbamazepinem indukovaných kožních nežádoucích účinků včetně SJS a TEN, vyrážky s eozinofilií (DRESS) nebo méně závažné akutní generalizované exantematózní pustulózy (AGEP) a makulopapulární vyrážky u lidé evropského a japonského původu.
Frekvence alely HLA-A * 3101 se mezi etnickými populacemi velmi liší. Alela HLA-A * 3101 má prevalenci 2 až 5% v evropské populaci a přibližně 10% v japonské populaci.
Přítomnost alely HLA-A * 3101 může zvýšit riziko karbamazepinem indukovaných kožních reakcí (většinou méně závažných) z 5,0% v obecné populaci na 26,0% u subjektů evropského původu, zatímco její absence může snížit riziko z 5,0 % až 3,8%.
Neexistují dostatečné údaje na podporu doporučení pro screening na HLA-A * 3101 před zahájením léčby karbamazepinem nebo chemicky příbuznými látkami.
Pokud se u pacientů evropského nebo japonského původu zjistí, že jsou pozitivní na alelu HLA-A * 3101, mělo by být použití karbamazepinu nebo chemicky příbuzných látek zvažováno pouze tehdy, pokud očekávaný přínos převáží rizika.
Omezení genetického screeningu
Genetický screening by nikdy neměl nahradit „adekvátní klinické pozorování a správu pacienta. Mnoho HLA-B * 1502 pozitivních asijských pacientů léčených Tolepem nevyvolá SJS / TEN a u pacientů s jakoukoli etnickou negativitou na HLA-B * 1502.“ HLA-B * Alela 1502, ale mohou se objevit epizody SJS / TEN. Podobně mnoho pacientů, kteří jsou pozitivní na alelu HLA-A * 3101 a jsou léčeni Tolepem, nevyvine SJS, TEN, DRESS, AGEP nebo makulopapulární vyrážku a u pacientů s jakákoli etnická negativita pro alelu HLA-A * 3101, nicméně mohou nastat tyto závažné kožní nežádoucí reakce.
Hyponatrémie
Sérové hladiny sodíku pod 125 mmol / l, obecně asymptomatické a nevyžadující úpravu léčby, byly pozorovány až u 2,7% pacientů léčených Tolepem. Výsledky z klinických studií ukazují, že sérové hladiny sodíku se po snížení dávky Tolepu, při přerušení dávkování nebo při konzervativním léčbě pacienta (např. Omezením příjmu tekutin) vrátí k normálu U pacientů s již existující renální dysfunkcí spojenou s nízkými hladinami sodíku nebo u pacientů léčených souběžně léky snižujícími sodík (např. diuretiky, desmopresinem) a také nesteroidními protizánětlivými léky (např. indomethacin), by měly být hladiny sodíku v séru měřeny před zahájením terapie Sérové hladiny sodíku by proto měly být měřeny při přibližně dva týdny a poté v měsíčních intervalech během prvních tří měsíců léčby, nebo podle potřeby klinicky.Tyto rizikové faktory mohou postihnout zejména starší pacienty.
Pacienti již na Tolep, kteří zahájí léčbu léky, které snižují hladinu sodíku, by měli podstoupit stejné kontroly hladin sodíku v séru. Obecně platí, že pokud se během léčby přípravkem Tolep vyskytnou příznaky naznačující hyponatrémii (viz bod 4.8), lze rozhodnout o měření hladin sodíku v séru. U ostatních pacientů mohou být tyto testy součástí běžných laboratorních kontrol.
Všem pacientům se srdečním selháním a sekundárním srdečním selháním by měla být pravidelně kontrolována váha, aby se ujistil, že nedochází k zadržování tekutin. V případě zadržování tekutin nebo zhoršení srdečních stavů by měly být monitorovány hladiny sodíku v séru. Pokud je pozorována hyponatrémie, může snížení příjmu tekutin představovat „důležité protiopatření. Protože léčba oxkarbazepinem může ve velmi vzácných případech vést ke zhoršení srdečního vedení, musí být pacienti s již existujícími poruchami vedení (např. Ventrikulární, arytmie) pečlivě sledován.
Funkce jater
Byly hlášeny velmi vzácné epizody hepatitidy, které ve většině případů příznivě odezněly. Pokud je podezření na jaterní účinek, je třeba sledovat jaterní funkce a zvážit přerušení léčby přípravkem Tolep.
Hematologické účinky
U pacientů léčených přípravkem Tolep po uvedení na trh byly hlášeny velmi vzácné případy agranulocytózy, aplastické anémie a pancytopenie (viz bod 4.8).
Pokud se objeví známky výrazného útlumu kostní dřeně, je třeba zvážit přerušení léčby.
Hormonální antikoncepce
Pacientky ve fertilním věku by měly být poučeny o tom, že souběžné používání přípravku Tolep a hormonální antikoncepce může jeho účinek zrušit (viz bod 4.5). Během léčby Tolepem se doporučuje používat alternativní nehormonální antikoncepční metody.
Alkohol
Extrémní opatrnost je vyžadována při konzumaci alkoholických nápojů během užívání Tolepu kvůli možnému aditivnímu sedativnímu účinku.
Sebevražedné myšlenky a chování
U pacientů užívajících antiepileptika v různých indikacích byly hlášeny případy sebevražedných představ a chování. Metaanalýza randomizovaných klinických studií versus placebo rovněž zdůraznila přítomnost mírného zvýšení rizika sebevražedných představ a chování.
Mechanismus tohoto rizika nebyl stanoven a dostupné údaje nevylučují možnost zvýšeného rizika u přípravku Tolep.
Pacienti by proto měli být sledováni z hlediska známek sebevražedných myšlenek a chování a v takovém případě by měla být zvážena vhodná léčba. Pacienti (a pečovatelé) by měli být poučeni, aby informovali svého ošetřujícího lékaře, pokud se objeví známky sebevražedných myšlenek nebo chování.
Přerušení léčby
Stejně jako u jiných antiepileptik by léčba přípravkem Tolep měla být ukončena postupně, aby se minimalizovalo riziko zvýšené frekvence záchvatů.
04.5 Interakce s jinými léčivými přípravky a jiné formy interakce
Indukce enzymů
Oxkarbazepin a jeho farmakologicky aktivní metabolit (monohydroxyderivát MHD) jsou slabé induktory in vitro A in vivo enzymů cytochromu P450 CYP3A4 a CYP3A5, odpovědných za metabolismus mnoha léčiv, jako jsou imunosupresiva (např. cyklosporin, takrolimus), perorální kontraceptiva (viz níže) a některá další antiepileptika (např. karbamazepin), což má za následek pokles plazmy hladiny těchto léčivých přípravků (viz tabulka níže, která shrnuje interakce s jinými antiepileptickými léčivými přípravky).
In vitro oxkarbazepin a MHD jsou slabými induktory enzymu UDP-glukuronyltransferázy (účinky na specifické enzymy patřící do této rodiny nejsou známy). in vivo Oxkarbazepin a MHD mohou mít malý indukční účinek na metabolismus léčivých přípravků, které jsou eliminovány hlavně po konjugaci pomocí enzymu UDP-glukuronyltransferázy. Při zahájení léčby nebo změně dávky Tolepu může nová úroveň indukce trvat 2 až 3 týdny .
Po přerušení léčby přípravkem Tolep může být po příslušném klinickém hodnocení a / nebo monitorování plazmatické hladiny nutné snížení dávky souběžně podávaných léčivých přípravků. Indukce pravděpodobně postupně klesá po dobu 2 až 3 týdnů po ukončení léčby.
Hormonální antikoncepce: Bylo prokázáno, že tolep ovlivňuje dvě složky perorální antikoncepce, ethinylestradiol (EE) a levonorgestrel (LNG). Průměrné hodnoty AUC EE a LNG se snižují o 48-52%, respektive o 32-52% . Proto může současné užívání přípravku Tolep a hormonální antikoncepce způsobit, že tyto přípravky budou neúčinné (viz bod 4.4) .Měly by být zváženy jiné způsoby antikoncepce, jiné než hormonální.
Enzymatická inhibice
Oxkarbazepin a MHD inhibují CYP2C19. Proto mohou při současném podávání vysokých dávek přípravku Tolep a léčivých přípravků metabolizovaných CYP2C19 (např. Fenytoin) docházet k interakcím. Plazmatické hladiny fenytoinu se po podání Tolepu v dávkách vyšších než 1200 mg / den zvyšují až o 40% (viz tabulka níže, která shrnuje interakce s jinými antiepileptiky). V tomto případě může být nutné snížení dávky fenytoinu (viz bod 4.2).
Antiepileptické léky
Během klinických studií byly pozorovány potenciální interakce mezi přípravkem Tolep a jinými antiepileptiky. Vliv těchto interakcí na průměrné hodnoty AUC a Cmin jsou shrnuty v následující tabulce.
Souhrn interakcí mezi přípravkem Tolep a jinými antiepileptiky
* Předběžné výsledky naznačují, že oxkarbazepin může vést ke snížení koncentrací lamotriginu, což může být u dětí důležité. Zdá se však, že tato potenciální interakce oxkarbazepinu je menší než ta, která byla pozorována při souběžném podávání léků indukujících enzymy, jako je karbamazepin, fenobarbital a fenytoin.
Silné induktory enzymů cytochromu P450 (tj. Karbamazepin, fenytoin a fenobarbital) jsou schopné snížit plazmatické hladiny MHD u dospělých (29–40%); u dětí ve věku od 4 do 12 let se clearance MHD zvyšuje přibližně o 35%, když je podáván jeden ze tří antiepileptik indukujících enzymy, ve srovnání s monoterapií. Souběžná léčba přípravkem Tolep a lamotriginu byla spojena se zvýšeným rizikem nežádoucích účinků (nauzea, somnolence, závratě a bolesti hlavy). Pokud je s Tolepem podáván jeden nebo více antiepileptických léčivých přípravků, může být podle potřeby nutná opatrná úprava dávky a / nebo monitorování plazmatických hladin, zvláště u pediatrických pacientů souběžně léčených lamotriginem.
U Tolepu nebyly pozorovány žádné samoindukční jevy.
Interakce s jinými léky
Cimetidin, erythromycin, viloxazin, warfarin a dextropropoxyfen nemají žádný vliv na farmakokinetiku MHD.
Interakce mezi oxkarbazepinem a inhibitory MAO je teoreticky možná na základě strukturálního vztahu mezi oxkarbazepinem a tricyklickými antidepresivy.
Do klinických studií byli zařazeni pacienti na tricyklické antidepresivní terapii a nebyly pozorovány žádné klinicky významné interakce.
Podávání oxkarbazepinu a lithia může způsobit zvýšenou neurotoxicitu.
04.6 Těhotenství a kojení
Těhotenství
Rizika spojená s epilepsií a antiepileptiky obecně:
Pacientkám, které mohou otěhotnět nebo jsou v plodném věku, by měla být poskytnuta odborná pomoc.
Pokud pacientka plánuje otěhotnět, měla by být přehodnocena potřeba antiepileptické léčby.
Bylo prokázáno, že u osob narozených ženám s epilepsií je výskyt malformací dvakrát až třikrát vyšší než při frekvenci přibližně 3% běžné populace.V ošetřované populaci nebyl pozorován nárůst malformací s polyterapií. bylo objasněno, do jaké míry je za nemoc zodpovědná léčba.
Účinná antiepileptická terapie by navíc neměla být přerušována, protože zhoršení onemocnění je škodlivé jak pro matku, tak pro plod.
Rizika spojená s oxkarbazepinem:
Klinické údaje o expozici během těhotenství jsou stále nedostatečné k posouzení teratogenního potenciálu oxkarbazepinu. Ve studiích na zvířatech byl při dávkách toxických pro matku pozorován zvýšený výskyt embryonální úmrtnosti, zpomalení růstu a přítomnost malformací (viz bod 5.3).
Vezmeme -li v úvahu toto vše:
- Pokud pacientky užívající přípravek Tolep otěhotní nebo plánují otěhotnět, je třeba použití tohoto přípravku pečlivě přehodnotit. Je třeba podávat nejnižší účinné dávky a upřednostňuje se monoterapie, pokud je to možné, alespoň během prvních tří měsíců těhotenství. ...
- Pacienti by měli být upozorněni, že se může zvýšit riziko malformací, a měli by být schopni podstoupit prenatální screening.
- Během těhotenství by neměla být účinná antiepileptická léčba oxkarbazepinem přerušena, protože zhoršení onemocnění je škodlivé jak pro matku, tak pro plod.
Monitorování a prevence
Antiepileptika mohou přispět k nedostatku kyseliny listové, což je jeden z možných faktorů odpovědných za abnormality plodu. Před a během těhotenství se doporučuje doplňkové podávání kyseliny listové. Vzhledem k tomu, že účinnost tohoto doplňkového podávání není prokázána, je možné u žen na doplňkové léčbě kyselinou listovou uvažovat o vhodnosti specifické prenatální diagnostiky.
Údaje od omezeného počtu žen naznačují, že během těhotenství v důsledku fyziologických změn, ke kterým dochází, mohou plazmatické hladiny aktivního metabolitu oxkarbazepinu (monohydroxylovaného derivátu, MHD) postupně klesat. Proto se u žen podstupujících léčbu Tolepem během těhotenství doporučuje pečlivě sledovat klinickou odpověď a zvážit sledování plazmatických koncentrací MHD, aby byla zajištěna adekvátní kontrola záchvatů během těhotenství. Po porodu lze také zvážit sledování plazmatických koncentrací MHD, zvláště pokud byly dávky léčiva během těhotenství zvýšeny.
U novorozence
U novorozenců byly hlášeny poruchy krvácení způsobené antiepileptiky. Preventivně by měl být vitamín K1 podáván k preventivním účelům v posledních týdnech těhotenství a následně novorozencům.
Čas krmení
Oxkarbazepin a jeho aktivní metabolit (MHD) se vylučují do mateřského mléka. U obou sloučenin byl poměr koncentrace mléka a plazmy 0,5. Účinky na novorozence vystavené Tolepu tímto způsobem nejsou známy. Tolep by proto neměl být užíván během kojení.
04.7 Účinky na schopnost řídit a obsluhovat stroje
Použití přípravku Tolep bylo spojeno s nástupem nežádoucích účinků, jako je závratě a ospalost (viz bod 4.8). Pacienti by proto měli být upozorněni, že by mohly být narušeny jejich fyzické a / nebo mentální schopnosti potřebné k řízení nebo obsluze strojů.
04.8 Nežádoucí účinky
Nejčastěji hlášenými nežádoucími účinky jsou somnolence, bolest hlavy, závratě, diplopie, nauzea, zvracení a únava, které se vyskytly u více než 10% pacientů.
Níže popsané nežádoucí účinky podle systému se týkají nežádoucích účinků hlášených v hodnocených klinických studiích souvisejících s léčbou přípravkem Tolep. Kromě toho byly posouzeny klinicky významné zprávy o nežádoucích účincích z programů farmakovigilance po uvedení přípravku na trh a programů ze soucitu.
Odhad frekvence *: Velmi časté: ≥ 1/10; Běžný: ≥ 1/100 - ≥ 1/1.000 - ≥ 1/10.000 -
V každé frekvenční třídě jsou nežádoucí účinky hlášeny sestupně podle závažnosti.
* na základě frekvenční klasifikace CIOMS III
† Klinicky významná hyponatrémie (sodík
Nežádoucí účinky ze spontánních hlášení a literatury (frekvence není známa)
Následující nežádoucí účinky pocházejí z postmarketingových zkušeností s přípravkem Tolep a odkazují na spontánní hlášení a případy popsané v literatuře. Protože tyto reakce vznikají spontánně z populace nejisté velikosti, není možné s jistotou odhadnout frekvenci, která je proto indikována. ... jako „není známo“. Nežádoucí účinky jsou seřazeny podle tříd orgánových systémů MedDRA. V každé třídě jsou nežádoucí účinky seřazeny podle klesající závažnosti.
Poruchy imunitního systému
Drogová vyrážka s eozinofilií a systémovými příznaky (DRESS).
Poruchy kůže a podkožní tkáně
Akutní generalizovaná exantematózní pustulóza (AGEP).
Poruchy svalové a kosterní soustavy a pojivové tkáně
Byly hlášeny případy snížení kostní minerální denzity, osteopenie, osteoporózy a zlomenin u pacientů dlouhodobě léčených přípravkem Tolep. Mechanismus, kterým Tolep ovlivňuje metabolismus kostí, nebyl identifikován.
04.9 Předávkování
Byly hlášeny ojedinělé případy předávkování. Maximální užitá dávka byla přibližně 24 000 mg. Všichni pacienti se zotavili pouze se symptomatickou léčbou. Příznaky předávkování zahrnují ospalost, závratě, nevolnost, zvracení, hyperkinezi, hyponatrémii, ataxii a nystagmus. Neexistuje žádné specifické antidotum.Pacienti s příznaky otravy v důsledku předávkování Tolepem by měli být léčeni vhodnou symptomatickou a podpůrnou terapií a lék by měl být volitelně odstraněn výplachem žaludku a / nebo inaktivován podáním aktivního uhlí.
05.0 FARMAKOLOGICKÉ VLASTNOSTI
05.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: antiepileptikum, derivát karboxamidu, ATC kód: N03AF02
Aktivní složka Tolepu oxkarbazepin a jeho 10-monohydroxylovaný metabolit mají antiepileptický účinek.
Obě účinné látky byly v sérii farmakologických studií na zvířatech prokázány jako silné a účinné antikonvulziva.
Kromě toho v modelu „vzteklá kočka“ získané výsledky svědčí o potenciálním psychotropním účinku na člověka.
Studie na zvířatech, které se týkají spektra aktivity oxkarbazepinu, ukazují na zvláštní účinnost u parciálních a generalizovaných tonicko-klonických záchvatů.
Antikonvulzivní mechanismus účinku oxkarbazepinu a jeho hlavního metabolitu byl objasněn pouze částečně; věří se však, že podobně jako karbamazepin tyto látky stabilizují přebuzené neuronální membrány, inhibují opakující se neuronální výboje a přenos synaptických impulzů.
Účinná látka přípravku Tolep nevykazuje vlastní indukci: farmakokinetika oxkarbazepinu a jeho farmakologicky aktivního metabolitu se po opakovaném podávání nemění. .
Není patrný žádný vliv Tolepu na stopu EEG.
Tolep je vhodný jak jako monoterapie, tak v kombinaci s jinými antiepileptiky (např. Valproátem, fenytoinem).
05.2 Farmakokinetické vlastnosti
Vstřebávání
Rychlá a prakticky úplná absorpce, maximálně 95%.
Plazmatická koncentrace: v důsledku rychlého metabolismu je plazmatická koncentrace oxkarbazepinu zanedbatelná a převládá farmakologicky aktivní metabolit (10-hydroxy-10,11-dihydro-5-karbamoyl-5H-dibenzazepin = 10-monohydroxyderivát).
Po jednorázových perorálních dávkách 150-600 mg oxkarbazepinu vykazuje plazmatická AUC 10-monohydroxy metabolitu lineární korelaci s podanou dávkou.
U pacientů s epilepsií způsobují denní dávky oxkarbazepinu v rozmezí od 600 do 5400 mg ustálené plazmatické koncentrace aktivního metabolitu v rozmezí od 2,1 do 36,7 μg / ml. Plazmatických píků aktivního metabolitu je dosaženo po jednorázovém podání do 4 hodin. Farmakokinetika oxkarbazepinu a jeho aktivního metabolitu zůstává i po opakovaném perorálním podání nezměněna.
U dětí jsou koncentrace v ustáleném stavu srovnatelné s koncentracemi u dospělých.
Rozdělení
Distribuční objem: 0,8 l / kg (aktivní metabolit).
Vazba na bílkoviny: 38% (aktivní metabolit).
Metabolismus
Oxkarbazepin se rychle z velké části redukuje na svůj farmakologicky aktivní metabolit, 10-monohydroxyderivát (přítomný jak volný, tak konjugovaný, což představuje asi 60% sloučenin vylučovaných ledvinami).
Drobné metabolity: přímý glukuronid a síran oxkarbazepinu a metabolit 10,11-dihydroxy (každý přibližně 5–15%). Nezměněný oxkarbazepin: méně než 0,3%.
Odstranění
Úplné vyřazení do 10 dnů. Více než 95% podané dávky se vylučuje močí, většinou ve formě metabolitů; asi 3% s výkaly.
Eliminační poločas 8-13 hodin (aktivní metabolit).
05.3 Předklinické údaje vztahující se k bezpečnosti
Předklinické údaje získané ze studií toxicity po opakovaném podávání, farmakologické bezpečnosti a genotoxicity provedených s oxkarbazepinem a jeho farmakologicky aktivním metabolitem (monohydroxylovaný derivát, MHD) neodhalily žádné zvláštní riziko pro člověka.
Příznaky nefrotoxicity byly pozorovány ve studiích opakovaných dávek prováděných na potkanech, nikoli však na myších a psech. Jelikož podobné účinky nebyly hlášeny u lidí, klinický význam těchto nálezů u potkanů zůstává neznámý.
Imunostimulační testy prováděné na myších ukázaly, že MHD (a v menší míře oxkarbazepin) může vyvolat opožděnou přecitlivělost.
Studie na zvířatech odhalily při dávkách toxických pro matku zvýšení výskytu embryonální mortality a někdy i ante a / nebo postnatální retardaci růstu. V jedné z osmi studií embryonální toxicity provedených s oxkarbazepinem a jeho farmakologicky aktivním metabolitem (MHD) došlo ke zvýšení u fetálních malformací u potkanů došlo v dávkách, které byly také toxické pro matku (viz bod 4.6).
Ve studiích karcinogenity byly u ošetřených zvířat indukovány nádory jater (krysy a myši), varlata a zrnité buňky ženského genitálního traktu (krysa). Výskyt jaterních nádorů byl s největší pravděpodobností důsledkem indukce jaterních mikrozomálních enzymů, což je indukční účinek, který, i když to nelze vyloučit, je u pacientů léčených Tolepem slabý nebo chybí. Nádory varlat mohou být vyvolány vysokými koncentracemi luteinizace Vzhledem k tomu, že toto zvýšení nebylo u lidí zjištěno, má se za to, že tyto nádory nemají žádný klinický význam. Ve studii kancerogenity provedené s MHD na potkanech bylo pozorováno na dávce závislé zvýšení výskytu nádorů granulárních buněk ženského genitálního traktu (děložního hrdla a pochvy). Tyto účinky se objevily při expozičních hladinách srovnatelných s těmi, které se v praxi očekávají. vývoj těchto nádorů nebyl objasněn, proto klinický význam těchto nádorů není znám.
06.0 FARMACEUTICKÉ INFORMACE
06.1 Pomocné látky
Koloidní bezvodý oxid křemičitý, mikrokrystalická celulóza, hypromelosa, červený oxid železitý, žlutý oxid železitý, stearan hořečnatý, sodná sůl karmelózy.
06.2 Neslučitelnost
Není známo.
06.3 Doba platnosti
3 roky.
06.4 Zvláštní opatření pro skladování
Tento léčivý přípravek nevyžaduje žádné zvláštní podmínky uchovávání.
06.5 Charakter vnitřního obalu a obsah balení
Netoxické blistry z PVC nebo PVC / PCTFE
Krabička s 50 dělitelnými tabletami po 300 mg.
Krabička s 50 dělitelnými tabletami po 600 mg.
06.6 Návod k použití a zacházení
Žádné zvláštní pokyny.
07.0 DRŽITEL ROZHODNUTÍ O REGISTRACI
Novartis Farma S.p.A.
Largo Umberto Boccioni, 1 - 21040 Origgio (VA)
08.0 REGISTRAČNÍ ČÍSLO
TOLEP 300 mg tablety - 50 dělitelných tablet A.I.C. č.: 028304018
TOLEP 600 mg tablety - 50 dělitelných tablet A.I.C. č.: 028304020
09.0 DATUM PRVNÍ REGISTRACE NEBO PRODLOUŽENÍ REGISTRACE
První povolení: 31.10.1994
Obnovení: 15.11.2009
10.0 DATUM REVIZE TEXTU
Stanovení AIFA ze dne 04.04.2014